Bahan aktif: Asetorfan
Tiorfix 10 mg butiran untuk suspensi oral
Sisipan paket Tiorfix tersedia untuk ukuran paket:- Tiorfix 10 mg butiran untuk suspensi oral
- Tiorfix 30 mg butiran untuk suspensi oral
- Tiorfix 100 mg kapsul
Indikasi Mengapa Tiorfix digunakan? Untuk apa?
Tiorfix adalah obat untuk pengobatan diare.
Tiorfix digunakan untuk pengobatan gejala diare akut pada anak di atas usia tiga bulan. Ini harus dikaitkan dengan asupan cairan yang melimpah dan dengan tindakan diet biasa, ketika tindakan ini saja tidak cukup efektif untuk mengendalikan diare, dan ketika pengobatan kausal tidak memungkinkan.
Racecadotril dapat diberikan sebagai pengobatan komplementer ketika pengobatan kausal memungkinkan.
Kontraindikasi Ketika Tiorfix tidak boleh digunakan
Jangan berikan Tiorfix
- Jika anak alergi (hipersensitif) terhadap racecadotril atau bahan lain dari Tiorfix.
- Jika dokter Anda telah memberi tahu Anda bahwa anak Anda tidak toleran terhadap beberapa gula, tanyakan kepada dokter Anda sebelum memberikan Tiorfix kepada anak Anda.
Kewaspadaan penggunaan Apa yang perlu Anda ketahui sebelum menggunakan Tiorfix
Bicaralah dengan dokter atau apoteker Anda sebelum memberikan Tiorfix kepada anak Anda.
Beri tahu dokter Anda jika:
- Bayi Anda berusia kurang dari tiga bulan,
- Temukan darah atau nanah di tinja bayi dan bayi demam. Penyebab diare bisa menjadi "infeksi bakteri yang perlu ditangani oleh dokter.
- Anak Anda mengalami diare kronis atau diare yang disebabkan oleh antibiotik,
- Anak Anda menderita penyakit ginjal atau gangguan fungsi hati,
- Anak Anda menderita muntah yang berkepanjangan atau tidak terkontrol,
- Anak Anda menderita diabetes (lihat "Informasi penting tentang beberapa bahan Tiorfix").
Interaksi Obat atau makanan mana yang dapat mengubah efek Tiorfix?
Beri tahu dokter Anda jika anak Anda sedang atau baru saja mengonsumsi obat lain, termasuk obat yang diperoleh tanpa resep.
Peringatan Penting untuk diketahui bahwa:
Kehamilan, menyusui dan kesuburan
Penggunaan Tiorfix tidak dianjurkan jika Anda sedang hamil atau menyusui.Bicaralah dengan dokter atau apoteker Anda sebelum minum obat apapun.
Mengemudi dan menggunakan mesin
Tiorfix tidak memiliki atau pengaruh yang dapat diabaikan pada kemampuan mengemudi atau menggunakan mesin.
Informasi penting tentang beberapa bahan dari Tiorfix
Tiorfix mengandung sekitar 1 g sukrosa per sachet.
Jika dokter Anda telah memberi tahu Anda bahwa bayi Anda tidak toleran terhadap beberapa gula, hubungi dia sebelum memberikan Tiorfix kepada bayi Anda.
Pada bayi dengan diabetes, jika dokter Anda meresepkan Tiorfix lebih dari 5 sachet per hari (setara dengan lebih dari 5 g sukrosa), hal ini harus diperhitungkan saat menghitung total asupan gula harian bayi.
Dosis, Cara dan Waktu Pemberian Cara Pemakaian Tiorfix: Posology
Tiorfix disediakan dalam bentuk butiran.
Butiran harus ditambahkan ke makanan atau dilarutkan dalam segelas air atau dalam botol bayi, dicampur dengan baik dan segera diberikan.
Dosis harian yang direkomendasikan tergantung pada berat badan anak: 1,5 mg / kg per dosis (sama dengan 1 atau 2 sachet), tiga kali sehari secara berkala.
Pada bayi dengan berat kurang dari 9 kg: satu sachet per dosis.
Pada bayi dari 9 kg hingga 13 kg: dua sachet per dosis.
Selalu berikan Tiorfix kepada anak Anda persis seperti yang dikatakan dokter Anda. Jika ragu, konsultasikan dengan dokter atau apoteker Anda.
Dokter Anda akan memberi tahu Anda berapa lama untuk melanjutkan pengobatan dengan Tiorfix. Ini harus dilanjutkan sampai bayi mengeluarkan dua tinja normal, selambat-lambatnya 7 hari.
Untuk mengkompensasi kehilangan cairan akibat diare, obat ini harus digunakan bersama dengan "suplemen cairan dan garam (elektrolit) yang cukup. Suplemen cairan dan garam terbaik dicapai dengan apa yang disebut larutan rehidrasi oral (jika ragu, silakan hubungi kami) tanyakan kepada dokter atau apoteker Anda).
Overdosis Apa yang harus dilakukan jika Anda terlalu banyak mengonsumsi Tiorfix?
Jika Anda menggunakan lebih banyak Tiorfix dari yang seharusnya
Jika anak Anda mengonsumsi Tiorfix lebih banyak dari yang seharusnya, segera hubungi dokter atau apoteker Anda.
Jika Anda lupa minum Tiorfix
Jangan beri anak Anda dosis ganda untuk mengganti dosis yang terlupakan. Lanjutkan perawatan seperti biasa.
Efek Samping Apa efek samping dari Tiorfix?
Seperti semua obat-obatan, obat ini dapat menyebabkan efek samping, meskipun tidak semua orang mendapatkannya.
Efek samping yang tidak biasa berikut telah dilaporkan (mereka memengaruhi 1 hingga 10 pengguna dalam 1000): tonsilitis (radang amigdala), ruam dan eritema (kemerahan pada kulit).
Efek samping lainnya (frekuensi yang tidak dapat diperkirakan dari data yang tersedia) adalah: eritema multiforme (lesi merah muda di ekstremitas dan di dalam mulut), radang lidah, radang wajah, radang bibir, radang kelopak mata, angioedema (radang subkutan di berbagai bagian tubuh), urtikaria , eritema nodosum ( peradangan berupa benjolan di bawah kulit), ruam papular (ruam kulit dengan lesi kecil, keras, kental), prurigo (lesi kulit gatal), gatal-gatal (sensasi gatal umum).
Berhenti memberikan Tiorfix kepada anak Anda segera dan hubungi dokter Anda segera jika anak Anda menunjukkan gejala angioedema, seperti:
- wajah bengkak, lidah atau faring
- kesulitan menelan
- gatal-gatal dan kesulitan bernafas
Jika salah satu efek samping menjadi serius atau jika Anda melihat ada efek samping yang tidak tercantum dalam selebaran ini, beri tahu dokter atau apoteker Anda.
Kadaluwarsa dan Retensi
Jauhkan dari jangkauan dan pandangan anak-anak.
Jangan gunakan Tiorfix setelah tanggal kedaluwarsa yang tertera pada kemasan sekunder setelah "EXP". Tanggal kedaluwarsa mengacu pada hari terakhir bulan itu.
Obat-obatan tidak boleh dibuang melalui air limbah atau limbah rumah tangga. Tanyakan apoteker Anda bagaimana cara membuang obat-obatan yang tidak lagi Anda gunakan. Ini akan membantu melindungi lingkungan.
Obat ini tidak memerlukan kondisi penyimpanan khusus.
Baca brosur paket sebelum digunakan.
Apa isi Tiorfix
Bahan aktifnya adalah racecadotril. Setiap sachet mengandung 10 mg racecadotril.
Bahan-bahan lainnya adalah:
Sukrosa,
silika koloid anhidrat,
Dispersi poliakrilat 30%,
Aroma aprikot
Seperti apa Tiorfix dan isi paketnya
Tiorfix disajikan dalam bentuk butiran untuk suspensi oral yang terkandung dalam sachet.
Setiap paket berisi 10, 16, 20, 30, 50, atau 100 sachet (pak berisi 100 sachet hanya untuk penggunaan di rumah sakit).
Tidak semua ukuran kemasan dapat dipasarkan
Sumber Paket Leaflet: AIFA (Badan Obat Italia). Konten yang diterbitkan pada Januari 2016. Informasi yang ada mungkin tidak up-to-date.
Untuk memiliki akses ke versi terbaru, disarankan untuk mengakses situs web AIFA (Badan Obat Italia). Penafian dan informasi yang berguna.
01.0 NAMA PRODUK OBAT
TIORFIX 10 MG GRANULS UNTUK SUSPENSI ORAL
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF
Setiap sachet mengandung 10 mg racecadotril.
Setiap sachet mengandung 966,5 mg sukrosa.
Untuk daftar lengkap eksipien, lihat bagian 6.1.
03.0 FORMULIR FARMASI
Butiran untuk suspensi oral.
Bubuk putih dengan bau aprikot yang khas.
04.0 INFORMASI KLINIS
04.1 Indikasi Terapi
Pengobatan simtomatik komplementer diare akut pada bayi (lebih dari 3 bulan) dan bayi, dalam kaitannya dengan rehidrasi oral dan tindakan suportif biasa, ketika tindakan tersebut saja tidak cukup untuk mengendalikan kondisi klinis, dan ketika pengobatan kausal tidak memungkinkan.
Jika pengobatan kausal memungkinkan, racecadotril dapat diberikan sebagai pengobatan komplementer.
04.2 Posologi dan cara pemberian
TIORFIX 10 mg diberikan secara oral, bersama dengan larutan rehidrasi oral (lihat bagian 4.4).
TIORFIX 10 mg ditujukan untuk anak-anak dengan berat badan
Dosis yang dianjurkan ditentukan berdasarkan berat badan: 1,5 mg / kg per dosis (sama dengan 1 atau 2 sachet), tiga kali sehari secara berkala.
Pada bayi dengan berat badan kurang dari 9 kg: satu sachet 10 mg 3 kali sehari.
Pada bayi dari 9 kg hingga 13 kg: 2 sachet 10 mg 3 kali sehari.
Durasi pengobatan dalam uji klinis pada anak-anak adalah 5 hari. Pengobatan harus dilanjutkan sampai dua pengeluaran feses yang normal dihasilkan. Perawatan tidak boleh lebih dari 7 hari. Pengobatan jangka panjang dengan racecadotril tidak dianjurkan.
Tidak ada studi klinis yang tersedia pada bayi kurang dari 3 bulan.
populasi khusus:
Tidak ada penelitian yang tersedia pada bayi atau anak-anak dengan gangguan ginjal atau hati (lihat bagian 4.4).
Perhatian dianjurkan pada pasien dengan gangguan hati atau ginjal.
Butiran dapat ditambahkan ke makanan, dilarutkan dalam segelas air atau dalam botol bayi, dicampur dengan baik dan segera diberikan.
04.3 Kontraindikasi
Hipersensitivitas terhadap zat aktif atau salah satu eksipien yang tercantum dalam bagian 6.1.
Produk obat ini mengandung sukrosa. Pasien dengan masalah herediter yang jarang dari intoleransi fruktosa, malabsorpsi glukosa-galaktosa atau insufisiensi sukrase-isomaltase tidak boleh minum obat ini.
04.4 Peringatan khusus dan tindakan pencegahan yang tepat untuk digunakan
Pemberian TIORFIX 10 mg tidak mengubah rejimen rehidrasi biasa. Sangat penting bahwa anak minum banyak cairan.
Dalam kasus diare parah atau berkepanjangan dengan muntah parah atau kehilangan nafsu makan, rehidrasi intravena harus dipertimbangkan.
Adanya tinja berdarah atau purulen dan demam dapat menunjukkan adanya bakteri invasif yang bertanggung jawab untuk diare atau adanya kondisi serius lainnya. Selain itu, Racecadotril belum diuji untuk diare terkait antibiotik. Oleh karena itu, Racecadotril tidak boleh diberikan dalam kondisi ini.
Ada penelitian yang cukup dalam pengobatan diare kronis dengan produk ini.
Untuk penderita diabetes harus diperhatikan bahwa setiap sachet mengandung 0,966 g sukrosa.
Jika jumlah sukrosa (sumber glukosa dan fruktosa) yang ada dalam dosis harian TIORFIX 10 mg melebihi 5 g per hari, ini harus diperhitungkan untuk dosis gula harian.
Produk tidak boleh diberikan kepada bayi di bawah usia 3 bulan karena tidak adanya studi klinis pada populasi ini.
Produk tidak boleh diberikan kepada anak-anak dengan gangguan ginjal atau hati, terlepas dari tingkat keparahannya, karena kurangnya informasi tentang populasi pasien ini.
Karena kemungkinan bioavailabilitas yang lebih rendah, produk tidak boleh diberikan jika terjadi muntah yang berkepanjangan atau tidak terkontrol.
04.5 Interaksi dengan produk obat lain dan bentuk interaksi lainnya
Tidak ada interaksi dengan bahan aktif lain pada manusia yang telah dijelaskan sampai saat ini.
Pada manusia, pengobatan bersamaan dengan racecadotril dan loperamide atau nifuroxazide tidak mengubah kinetika racecadotril.
04.6 Kehamilan dan menyusui
Kesuburan
Studi kesuburan yang dilakukan dengan racecadotril pada tikus Sprague-Dawley menunjukkan tidak ada dampak pada kesuburan.
Kehamilan
Tidak ada data yang memadai dari penggunaan racecadotril pada wanita hamil.Penelitian pada hewan belum menunjukkan efek berbahaya langsung atau tidak langsung sehubungan dengan kehamilan, kesuburan, perkembangan janin embrio, persalinan atau perkembangan pascakelahiran.Namun, karena tidak adanya. studi klinis yang tersedia, racecadotril tidak boleh diberikan kepada wanita hamil.
Waktunya memberi makan
Karena kurangnya informasi tentang sekresi racecadotril dalam ASI, produk obat ini tidak boleh diberikan kepada wanita menyusui.
04.7 Efek pada kemampuan mengemudi dan menggunakan mesin
Tidak berhubungan.
Racecadotril tidak memiliki atau pengaruh yang dapat diabaikan pada kemampuan mengemudi atau menggunakan mesin.
04.8 Efek yang tidak diinginkan
Data tersedia dari uji klinis yang melibatkan 860 pasien anak dengan diare akut yang diobati dengan racecadotril dan 441 yang diobati dengan plasebo.
Efek yang tidak diinginkan yang tercantum di bawah ini terjadi lebih sering dengan racecadotril dibandingkan dengan plasebo atau dilaporkan selama pengawasan pasca-pemasaran. Frekuensi efek yang tidak diinginkan didefinisikan menggunakan konvensi berikut: sangat umum (≥ 1/10), umum (≥ 1/100 hingga
Infeksi dan infestasi
Jarang: tonsilitis.
Gangguan kulit dan jaringan subkutan
Jarang: ruam, eritema.
Tidak diketahui: eritema multiforme, edema lingual, edema wajah, edema bibir, edema okular, angioedema, urtikaria, eritema nodosum, ruam papular, prurigo, pruritus.
04.9 Overdosis
Tidak ada kasus overdosis yang dilaporkan. Dosis tunggal lebih besar dari 2 g, setara dengan 20 kali dosis terapeutik, telah diberikan pada orang dewasa dan tidak ada efek berbahaya yang telah dijelaskan.
05.0 SIFAT FARMAKOLOGIS
05.1 Sifat farmakodinamik
Kelompok farmakoterapi: antidiare lainnya.
Kode ATC: A07XA04.
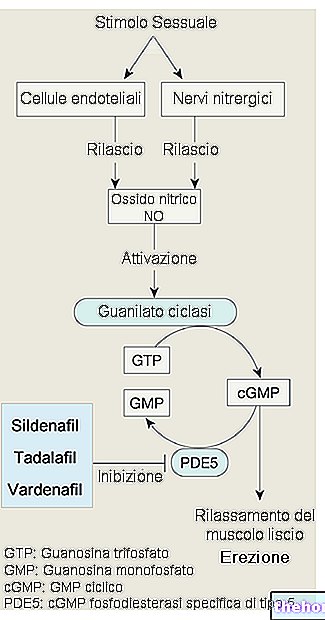
Racecadotril adalah prodrug yang harus dihidrolisis menjadi metabolit aktif thiorphan, yang merupakan inhibitor ensefalinase, enzim peptidase membran sel yang terletak di berbagai jaringan, terutama di epitel usus kecil. Enzim ini berkontribusi pada pencernaan peptida. degradasi peptida endogen, seperti enkephalins Racecadotril melindungi enkephalins dari degradasi enzimatik dengan memperpanjang aksinya pada tingkat sinapsis ensefalinergik di usus kecil dan mengurangi hipersekresi.
Racecadotril adalah bahan aktif antisekresi usus murni. Hal ini menyebabkan penurunan hipersekresi usus air dan elektrolit yang disebabkan oleh toksin kolera atau oleh keadaan inflamasi, dan tidak berpengaruh pada aktivitas sekresi basal Racecadotril memiliki aktivitas antidiare yang cepat, tanpa mengubah waktu transit usus..
Dalam dua uji klinis pada anak-anak, racecadotril mengurangi berat tinja masing-masing sebesar 40% dan 46%, dalam 48 jam pertama. Penurunan yang signifikan dalam durasi diare dan kebutuhan untuk rehidrasi juga diamati.
Sebuah meta-analisis (9 uji klinis acak racecadotril versus plasebo, selain larutan rehidrasi oral) mengumpulkan data pada pasien individu dari 1384 anak laki-laki dan perempuan dengan diare akut dengan tingkat keparahan yang bervariasi dan dirawat sebagai pasien rawat inap atau rawat jalan. Usia rata-rata adalah 12 bulan (kisaran interkuartil: 6 hingga 39 bulan). Sebanyak 714 pasien berusia kurang dari 1 tahun dan 670 pasien berusia 1 tahun atau lebih. pasien antara studi berkisar antara 7,4 kg hingga 12,2 kg. Durasi rata-rata diare setelah inklusi adalah 2,81 hari untuk kelompok plasebo dan 1,75 hari untuk kelompok racecadotril. Proporsi pasien rawat inap lebih tinggi pada kelompok racecadotril dibandingkan dengan plasebo [HR (Hazard Ratio): 2,04; 95% CI: 1,85 hingga 2,32; p 1 tahun) (HR: 2,16; 95% CI: 1,83 hingga 2,57; p
Racecadotril tidak menyebabkan distensi abdomen. Selama perkembangan klinisnya, racecadotril menyebabkan timbulnya konstipasi sekunder pada persentase pasien yang sebanding dengan yang terlihat dengan pemberian plasebo. Dalam kasus pemberian oral, aktivitas dilakukan secara eksklusif di tingkat perifer, tanpa efek pada sistem saraf pusat. .
Sebuah studi cross-over acak menunjukkan bahwa racecadotril 100 mg kapsul pada dosis terapeutik (1 kapsul) atau pada dosis supra-terapeutik (4 kapsul) tidak menginduksi perpanjangan interval QT / QTc pada 56 sukarelawan sehat (berlawanan dengan moksifloksasin, digunakan sebagai kontrol).
05.2 Sifat farmakokinetik
Penyerapan
Racecadotril cepat diserap setelah pemberian oral.
Distribusi
Dalam plasma, setelah dosis oral racecadotril berlabel C-14, paparan radiokarbon yang diukur jauh lebih tinggi daripada di sel darah dan 3 kali lebih tinggi daripada di seluruh darah. Oleh karena itu obat tidak mengikat sel darah pada tingkat yang signifikan. Distribusi radiokarbon ke jaringan tubuh lainnya adalah moderat, seperti yang ditunjukkan oleh rata-rata volume distribusi dalam plasma sebesar 66,4 kg.
Sembilan puluh persen metabolit aktif racecadotril (thiorfan = (RS) -N - (1-oxo -2 - (mercaptomethyl) -3 -phenylpropyl) glisin) terikat pada protein plasma, terutama albumin.
Durasi dan tingkat efek racecadotril bergantung pada dosis. Penghambatan ensefalinase plasma puncak dicapai dalam waktu sekitar 2 jam dan sesuai dengan penghambatan 90% dengan dosis 1,5 mg / kg. Durasi penghambatan ensefalinase plasma sekitar 8 jam.
Metabolisme
Waktu paruh racecadotril, dihitung sebagai penghambatan ensefalinase plasma, adalah sekitar 3 jam.
Racecadotril dengan cepat dihidrolisis menjadi thiorphan (RS) -N - (1 -oxy -2 - (mercaptomethyl) -3 -phenylpropyl) glisin, metabolit aktif, pada gilirannya diubah menjadi metabolit tidak aktif yang diidentifikasi sebagai S-methylthiorphan sulfoxide, thiorphan S -methyl , asam propionat 2-metanosulfinilmetil dan asam propionat 2-metilsulfanilmetil, semuanya terbentuk dengan paparan sistemik terhadap obat induk lebih besar dari 10%.
Metabolit minor lainnya juga terdeteksi dan diukur dalam urin dan feses.
Data in vitro menunjukkan bahwa racecadotril / thiorfan dan empat metabolit tidak aktif utama tidak menghambat isoform enzim CYP utama 3A4, 2D6, 2C9, 1A2 dan 2C19 pada tingkat yang relevan secara klinis.
Data in vitro menunjukkan bahwa racecadotril / thiorfan dan empat metabolit tidak aktif utama tidak menginduksi isoform enzim CYP (keluarga 3A, 2A6, 2B6, 2C9 / 2C19, keluarga 1A, 2E1) dan enzim terkonjugasi UGT pada tingkat yang relevan secara klinis.
Pada populasi anak-anak, hasil farmakokinetik serupa dengan populasi orang dewasa, dengan Cmax mencapai 2 jam dan 30 menit setelah pemberian dosis. Tidak ada akumulasi setelah beberapa dosis diberikan setiap 8 jam selama 7 hari.
Pengeluaran
Racecadotril dieliminasi dalam bentuk metabolit aktif dan tidak aktif. Ekskresi terjadi terutama melalui ginjal (81,4%) dan, pada tingkat yang jauh lebih rendah, melalui rute feses (sekitar 8%) Rute paru tidak signifikan (kurang dari 1% dari dosis).
05.3 Data keamanan praklinis
Studi toksisitas kronis 4 minggu pada monyet dan anjing, disesuaikan dengan durasi pengobatan pada manusia, menunjukkan tidak ada efek pada dosis hingga 1250 mg / kg / hari dan 200 mg / kg, sesuai dengan margin keamanan 625 dan 62 (sehubungan dengan untuk "manusia). Racecadotril tidak imunotoksik pada tikus yang diobati dengan racecadotril hingga 1 bulan. Paparan yang lebih lama (1 tahun) pada monyet menunjukkan infeksi umum dan penurunan respon antibodi dengan vaksinasi dengan dosis 500 mg/kg/hari dan tidak ada infeksi/imunosupresi dengan dosis 120 mg/kg/hari. Demikian juga, beberapa parameter infeksi / kekebalan bervariasi pada anjing yang diobati dengan 200 mg / kg / hari selama 26 minggu. Relevansi klinis tidak diketahui, lihat bagian 4.8.
Tidak ada efek mutagenik atau klastogenik dari racecadotril yang ditemukan dalam tes standar in vitro Dan in vivo.
Tes karsinogenisitas belum dilakukan dengan racecadotril karena obat ini ditujukan untuk pengobatan jangka pendek.
Toksisitas reproduksi dan perkembangan (studi tentang kesuburan dan perkembangan embrio awal, perkembangan prenatal dan postnatal termasuk fungsi ibu, perkembangan embrio-janin) tidak mengungkapkan efek spesifik untuk racecadotril.
Sebuah studi toksisitas pada tikus remaja mengungkapkan tidak ada efek signifikan dari racecadotril hingga dosis 160 mg / kg / hari, yang 35 kali lebih tinggi dari rejimen pediatrik biasa (yaitu 4,5 mg / kg / hari).
Meskipun fungsi ginjal belum matang pada bayi kurang dari 1 tahun, tingkat paparan yang lebih tinggi tidak diharapkan pada individu ini.
Efek praklinis lainnya (misalnya anemia berat, kemungkinan aplastik, peningkatan diuresis, ketonuria, diare) diamati hanya pada kasus paparan yang dianggap cukup melebihi paparan maksimum yang diharapkan pada manusia. Relevansi klinis tidak diketahui.
Studi farmakologi keamanan lainnya tidak mengungkapkan efek berbahaya racecadotril pada sistem saraf pusat dan pada fungsi kardiovaskular dan pernapasan.
Pada hewan, racecadotril menyebabkan peningkatan efek butilskopolamin pada transit usus dan efek antikonvulsan fenitoin.
06.0 INFORMASI FARMASI
06.1 Eksipien
Sukrosa
Silika koloid anhidrat
Dispersi poliakrilat 30%
Aroma aprikot.
06.2 Ketidakcocokan
Tidak berhubungan.
06.3 Masa berlaku
2 tahun.
06.4 Tindakan pencegahan khusus untuk penyimpanan
Obat ini tidak memerlukan kondisi penyimpanan khusus.
06.5 Sifat kemasan langsung dan isi kemasan
Kantong kertas / aluminium / polietilen yang disegel panas.
Kemasan 10, 16, 20, 30, 50 dan 100 sachet (100 sachet hanya untuk penggunaan di rumah sakit).
Tidak semua ukuran kemasan dapat dipasarkan.
06.6 Petunjuk penggunaan dan penanganan
Tidak ada instruksi khusus.
07.0 PEMEGANG OTORITAS PEMASARAN
BIOPROJET EROPA LTD
29 Teras Earlsfort,
2, Dublin
Irlandia
08.0 NOMOR OTORITAS PEMASARAN
AIC n. 037518115 / M "butiran 10 mg untuk suspensi oral" 10 sachet dalam kertas / Al / PE - anak usia dini
AIC n. 037518127 / M "butiran 10 mg untuk suspensi oral" 16 kertas / Al / PE sachet - anak usia dini 20
AIC n. 037518139 / M "butiran 10 mg untuk suspensi oral" 20 kertas / Al / PE sachet - anak usia dini 30
AIC n. 037518141 / M "butiran 10 mg untuk suspensi oral" 30 sachet kertas / Al / PE - anak usia dini 50
AIC n. 037518154 / M "butiran 10 mg untuk suspensi oral" 50 sachet kertas / Al / PE - anak usia dini
AIC n. 037518166 / M "butiran 10 mg untuk suspensi oral" 100 sachet kertas / Al / PE - anak usia dini
09.0 TANGGAL OTORISASI PERTAMA ATAU PEMBARUAN KUASA
/
10.0 TANGGAL REVISI TEKS
08/03/2013




















.jpg)