Apa itu Kadcyla dan untuk apa kegunaannya?
Kadcyla adalah obat kanker yang mengandung zat aktif trastuzumab emtansine. Ini digunakan untuk mengobati orang dewasa dengan kanker payudara stadium lanjut atau metastatik (kanker yang telah menyebar ke bagian lain dari tubuh) yang sebelumnya telah menerima pengobatan dengan trastuzumab dan taxane (sejenis obat kanker). Kadcyla hanya dapat digunakan ketika kanker telah terbukti "mengekspresikan" jumlah HER2 yang berlebihan, yaitu ketika sel kanker menghasilkan sejumlah besar protein pada permukaannya, yang disebut HER2 (faktor pertumbuhan epidermal manusia), yang merangsang pertumbuhan sel itu sendiri.
Bagaimana Kadcyla digunakan - trastuzumab emtansine?
Kadcyla hanya dapat diperoleh dengan resep dan pengobatan harus diresepkan oleh dokter dan diberikan di bawah pengawasan profesional kesehatan yang berpengalaman dalam perawatan pasien kanker. Ini tersedia sebagai bubuk untuk dibuat menjadi solusi untuk infus (tetes) ke dalam vena. Dosis yang akan diberikan tergantung pada berat badan pasien dan infus diulang setiap tiga minggu. Jika infus 90 menit pertama telah ditoleransi dengan baik, dosis berikutnya dapat diberikan dalam infus 30 menit. Terapi dapat dilanjutkan dengan lebih sedikit. bahwa penyakit tidak memburuk atau pasien tidak lagi mentoleransi pengobatan.
Selama infus dan segera setelah infus, pasien harus dipantau untuk reaksi terkait infus termasuk kemerahan, menggigil dan demam. Pada pasien yang mengalami reaksi alergi atau efek samping, dokter mungkin perlu mengurangi dosis atau menghentikan pengobatan dengan Kadcyla. Untuk informasi lebih lanjut, lihat brosur paket.
Bagaimana cara kerja Kadcyla - trastuzumab emtansine?
Zat aktif dalam Kadcyla, trastuzumab emtansine, terdiri dari dua komponen aktif yang digabungkan bersama:
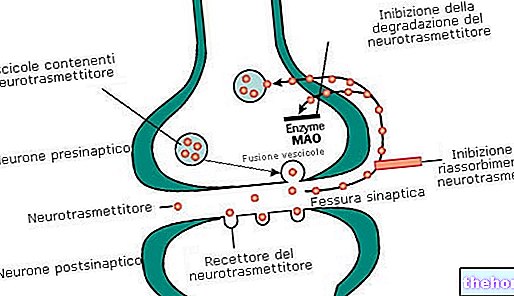
- trastuzumab, antibodi monoklonal (sejenis protein) yang dirancang untuk mengenali dan menempel pada protein HER2, yang terdapat dalam jumlah besar di permukaan beberapa sel kanker. Dengan menempel pada HER2, trastuzumab mengaktifkan sel-sel sistem kekebalan, yang kemudian menyerang sel kanker. Trastuzumab juga menghalangi HER2 untuk merangsang pertumbuhan sel kanker. Sekitar seperempat dari kanker payudara mengekspresikan jumlah HER2 yang berlebihan;
- DM1, zat beracun yang membunuh sel saat mereka mencoba membelah dan tumbuh. DM1 diaktifkan ketika Kadcyla memasuki sel kanker. Ini mengikat protein yang ditemukan dalam sel ("tubulin") yang penting dalam membentuk "kerangka" internal yang perlu diisi kembali oleh sel ketika mereka membelah. Dengan mengikuti tubulin dalam sel kanker, DM1 memblokir pembentukan kerangka, mencegah sel kanker membelah dan tumbuh.
Apa manfaat yang ditunjukkan Kadcyla - trastuzumab emtansine selama penelitian?
Kadcyla telah terbukti secara signifikan memperlambat memburuknya penyakit dan memperpanjang kelangsungan hidup pasien dengan kanker payudara stadium lanjut dan metastatik yang mengekspresikan HER2 yang sebelumnya telah menerima pengobatan dengan trastuzumab dan taxane. Dalam satu penelitian utama yang melibatkan 991 pasien, subjek yang diobati dengan Kadcyla bertahan selama rata-rata 9,6 bulan tanpa perkembangan penyakit dibandingkan dengan 6,4 bulan untuk pasien yang diobati dengan dua obat antikanker lainnya, capecitabine dan lapatinib. Selain itu, pasien yang diobati dengan Kadcyla bertahan 31 bulan dibandingkan dengan 25 bulan pada pasien yang diobati dengan capecitabine dan lapatinib.
Apa risiko yang terkait dengan Kadcyla - trastuzumab emtansine?
Efek samping yang paling umum dengan Kadcyla (yang dapat mempengaruhi lebih dari 25% pasien) adalah pendarahan (termasuk mimisan), peningkatan kadar transaminase darah (enzim hati), kelelahan, nyeri otot dan tulang, dan sakit kepala. Efek samping serius yang paling umum adalah demam (demam), trombositopenia (penurunan jumlah trombosit), muntah, sakit perut, mual, sembelit, diare, dispnea (kesulitan bernapas) dan pneumonia (radang paru-paru). Untuk daftar lengkap efek samping yang dilaporkan dengan Kadcyla, lihat brosur paket.
Mengapa Kadcyla - trastuzumab emtansine disetujui?
Komite Badan untuk Produk Obat untuk Penggunaan Manusia (CHMP) memutuskan bahwa manfaat Kadcyla lebih besar daripada risikonya dan merekomendasikannya agar disetujui untuk digunakan di UE. CHMP memperhitungkan peningkatan signifikan dalam kelangsungan hidup yang diamati. pada pasien yang diobati dengan Kadcyla dibandingkan dengan terapi standar Mengenai keamanan Kadcyla, efek samping keseluruhan dianggap dapat dikelola dan profil keamanan keseluruhan dianggap menguntungkan dibandingkan dengan obat-obatan yang tersedia saat ini.
Tindakan apa yang diambil untuk memastikan penggunaan Kadcyla - trastuzumab emtansine yang aman dan efektif?
Rencana manajemen risiko telah dikembangkan untuk memastikan bahwa Kadcyla digunakan seaman mungkin. Berdasarkan rencana ini, informasi keselamatan telah ditambahkan ke ringkasan karakteristik produk dan selebaran paket untuk Kadcyla, termasuk tindakan pencegahan yang tepat untuk diikuti oleh profesional kesehatan dan pasien. Karena potensi risiko kebingungan antara Kadcyla dan Herceptin, karena kesamaan nama zat aktif (trastuzumab emtansine dan trastuzumab), perusahaan akan memberikan materi pendidikan kepada semua profesional kesehatan yang mungkin menggunakan Kadcyla atau Herceptin, untuk menentukan bahwa obat-obatan tersebut tidak boleh digunakan secara bergantian dan untuk mengkomunikasikan tindakan yang harus diambil untuk menghindari kesalahan pengobatan.
Informasi lebih lanjut tentang Kadcyla - trastuzumab emtansine
Pada tanggal 15 November 2013, Komisi Eropa mengeluarkan "Otorisasi Pemasaran" untuk Kadcyla, berlaku di seluruh Uni Eropa. Untuk versi lengkap Kadcyla EPAR, silakan lihat situs web Badan: ema.Europa.eu / Temukan obat / Obat-obatan manusia / Laporan penilaian publik Eropa Untuk informasi lebih lanjut tentang terapi Kadcyla, baca selebaran paket (disertakan dengan EPAR) atau hubungi dokter atau apoteker Anda. Pembaruan terakhir dari ringkasan ini: 11-2013.
Informasi tentang Kadcyla - trastuzumab emtansine yang dipublikasikan di halaman ini mungkin kedaluwarsa atau tidak lengkap. Untuk penggunaan yang benar dari informasi ini, lihat halaman Penafian dan informasi yang berguna.