Bahan aktif: Ceftazidime
Starcef 250 mg / 1ml bubuk dan pelarut untuk larutan injeksi
Starcef 500 mg / 1,5 ml bubuk dan pelarut untuk larutan injeksi
Starcef 1 g / 3 ml bubuk dan pelarut untuk larutan injeksi
Indikasi Mengapa Starcef digunakan? Untuk apa?
Starcef adalah antibiotik yang digunakan pada orang dewasa dan anak-anak (termasuk bayi baru lahir). Ia bekerja dengan membunuh bakteri yang menyebabkan infeksi dan termasuk dalam kelompok obat yang disebut sefalosporin.
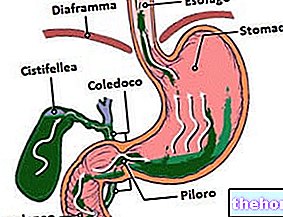
Starcef digunakan untuk mengobati infeksi bakteri parah pada:
- paru-paru atau dada
- paru-paru dan bronkus pada pasien yang menderita cystic fibrosis
- otak (meningitis)
- telinga
- saluran kemih
- kulit dan jaringan lunak
- perut dan dinding perut (peritonitis)
- tulang dan sendi.
Starcef juga dapat digunakan:
- untuk mencegah infeksi selama operasi prostat pada pria
- untuk mengobati pasien dengan jumlah sel darah putih rendah (neutropenia) yang mengalami demam karena 'infeksi bakteri.
Kontraindikasi Ketika Starcef tidak boleh digunakan
Anda tidak boleh diberikan Starcef:
- jika Anda alergi terhadap ceftazidime atau bahan lain dari obat ini.
- jika Anda memiliki reaksi alergi parah terhadap antibiotik lain (penisilin, monobaktam, dan karbapenem) karena Anda mungkin juga alergi terhadap Starcef.
- Beri tahu dokter Anda sebelum memulai perawatan dengan Starcef jika menurut Anda ini berlaku untuk Anda. Anda tidak harus diberikan Starcef.
Kewaspadaan Penggunaan Apa yang perlu Anda ketahui sebelum mengonsumsi Starcef
Berhati-hatilah dengan Starcef
Waspadai beberapa gejala seperti reaksi alergi, gangguan sistem saraf, dan gangguan pencernaan seperti diare saat diobati dengan Starcef. Ini akan mengurangi risiko kemungkinan masalah. Lihat (Kondisi yang perlu Anda perhatikan) di bagian 4. Jika Anda pernah mengalami reaksi alergi terhadap antibiotik lain, Anda mungkin juga alergi terhadap Starcef.
Jika Anda membutuhkan tes darah atau urin
Starcef dapat memengaruhi hasil tes keberadaan gula dalam urin dan tes darah yang dikenal sebagai tes Coombs. Jika Anda menjalani tes ini:
- Beri tahu orang yang mengambil sampel bahwa Anda sedang dirawat dengan Starcef.
Interaksi Obat atau makanan apa yang dapat mengubah efek Starcef
Beri tahu dokter Anda jika Anda sedang mengonsumsi, baru saja mengonsumsi atau mungkin sedang mengonsumsi obat lain. Ini juga termasuk obat-obatan tanpa resep.
Anda tidak boleh diberikan Starcef tanpa berkonsultasi dengan dokter Anda jika Anda sedang mengonsumsi:
- antibiotik yang disebut kloramfenikol
- sejenis antibiotik yang disebut aminoglikosida misalnya gentamisin, tobramycin
- tablet diuretik yang disebut furosemide
- Beri tahu dokter Anda jika ini berlaku untuk Anda.
Peringatan Penting untuk diketahui bahwa:
Kehamilan, menyusui dan kesuburan
Mintalah saran dokter Anda sebelum Anda diberikan Starcef:
- jika Anda sedang hamil, curiga, atau berencana untuk hamil
- jika Anda menyusui
Dokter Anda akan mempertimbangkan manfaat pengobatan dengan Starcef terhadap risiko pada bayi.
Mengemudi dan menggunakan mesin
Starcef dapat menyebabkan efek samping yang mempengaruhi kemampuan mengemudi seperti pusing. Jangan mengemudi atau menggunakan mesin kecuali Anda yakin tidak mengalami efek apa pun.
Starcef mengandung natrium
Anda perlu mempertimbangkan hal-hal berikut jika Anda menjalani diet natrium terkontrol.
Dosis, Cara dan Waktu Pemberian Cara Pemakaian Starcef: Posology
Starcef biasanya diberikan oleh dokter atau perawat. Ini dapat diberikan sebagai "infus intravena atau sebagai suntikan" langsung ke pembuluh darah atau otot.
Starcef disiapkan oleh dokter, apoteker, atau perawat Anda menggunakan air untuk injeksi atau cairan infus yang sesuai.
Dosis yang direkomendasikan
Dosis Starcef yang tepat akan ditentukan oleh dokter Anda dan tergantung pada: tingkat keparahan dan jenis infeksi; jika Anda sedang dirawat dengan antibiotik lain; berat badan dan usia Anda, kondisi ginjal Anda.
Bayi baru lahir (0-2 bulan): untuk setiap kg berat badan bayi, 25 hingga 60 mg Starcef akan diberikan per hari yang dibagi menjadi dua dosis.
Bayi (di atas 2 bulan) dan bayi dengan berat kurang dari 40 kg: untuk setiap kg berat badan bayi atau anak, 100 hingga 150 mg Starcef per hari akan diberikan dalam tiga dosis. Dosis maksimum adalah 6 g per hari.
Dewasa dan remaja dengan berat 40 kg atau lebih: 1 hingga 2 g Starcef tiga kali sehari. Dosis maksimum adalah 9 g per hari.
Pasien di atas 65 tahun: Dosis harian umumnya tidak boleh melebihi 3 g per hari terutama jika Anda berusia di atas 80 tahun.
Pasien dengan masalah ginjal: Anda mungkin diberikan dosis yang berbeda dari biasanya. Dokter atau perawat Anda akan memutuskan berapa banyak Starcef yang Anda butuhkan berdasarkan tingkat keparahan penyakit ginjal Anda.Dokter Anda akan memantau Anda dengan cermat dan mungkin melakukan tes fungsi ginjal secara berkala.
Jika lupa memakai Starcef : Jika lupa suntikan, harus segera diminum Jangan minum dosis ganda (dua suntikan sekaligus) untuk mengganti dosis yang terlupakan, ambil dosis berikutnya di waktu yang biasa.
Jangan berhenti minum Starcef: Jangan berhenti minum Starcef kecuali dokter Anda memberi tahu Anda. Jika Anda memiliki pertanyaan lebih lanjut tentang penggunaan obat ini, tanyakan kepada dokter atau perawat Anda.
Overdosis Apa yang harus dilakukan jika Anda terlalu banyak mengonsumsi Starcef
Jika Anda diberi Starcef lebih dari yang seharusnya: Jika Anda secara tidak sengaja menggunakan dosis yang lebih tinggi dari yang ditentukan, segera hubungi dokter atau rumah sakit terdekat.
Efek Samping Apa efek samping dari Starcef
Seperti semua obat-obatan, obat ini dapat menyebabkan efek samping, meskipun tidak semua orang mendapatkannya.
Kondisi yang perlu Anda waspadai Efek samping serius berikut telah terjadi pada sejumlah kecil orang, tetapi frekuensi pastinya tidak diketahui:
- Reaksi Alergi Berat. Tanda-tandanya termasuk ruam yang gatal, bengkak, kadang-kadang di wajah atau mulut yang menyebabkan kesulitan bernafas.
- ruam kulit dengan formasi melepuh kecil seperti target (bintik gelap di tengah dikelilingi oleh "area terang dengan cincin hitam di sekitar tepinya).
- ruam luas dengan lepuh dan pengelupasan kulit (ini mungkin tanda sindrom Stevens-Johnson atau nekrolisis epidermal toksik).
- gangguan sistem saraf: tremor, kejang dan, dalam beberapa kasus, koma. Ini telah terjadi pada orang yang dosisnya terlalu tinggi, terutama pada orang dengan penyakit ginjal.
- ada laporan yang jarang dari reaksi hipersensitivitas parah dengan ruam kulit yang parah, yang mungkin disertai dengan demam, kelelahan, pembengkakan pada wajah atau kelenjar getah bening, peningkatan eosinofil (sejenis sel darah putih), efek pada hati, ginjal atau paru-paru ( reaksi yang disebut DRESS, Reaksi Obat dengan Eosinofilia dan Gejala Sistemik).
Hubungi dokter atau perawat Anda segera jika Anda mendapatkan gejala-gejala ini
Efek samping yang umum
Ini dapat mempengaruhi hingga 1 dari 10 pasien:
- diare
- pembengkakan dan kemerahan di sepanjang vena
- timbul ruam merah yang mungkin gatal
- rasa sakit, terbakar, bengkak atau peradangan di tempat suntikan.
- Beri tahu dokter Anda jika salah satu dari kondisi ini mengkhawatirkan Anda.
Efek samping umum yang mungkin muncul dalam tes darah adalah:
- peningkatan jenis sel darah putih (eosinofilia)
- peningkatan jumlah sel yang membantu pembekuan darah
- peningkatan enzim hati.
Efek samping yang jarang terjadi
Ini dapat mempengaruhi hingga 1 dari 100 pasien:
- radang usus yang dapat menyebabkan rasa sakit atau diare yang mungkin mengandung darah
- kandidiasis - infeksi jamur di mulut atau vagina
- sakit kepala
- pusing
- sakit perut
- mual atau muntah
- demam dan menggigil.
- Beri tahu dokter Anda jika Anda memiliki salah satu dari kondisi ini.
Efek samping yang tidak umum yang mungkin muncul dalam tes darah adalah:
- penurunan jumlah sel darah putih
- pengurangan jumlah trombosit (sel yang membantu pembekuan darah)
- peningkatan kadar ureum, BUN atau kreatinin serum.
Efek samping yang sangat jarang terjadi
Ini dapat mempengaruhi hingga 1 dari 10.000 pasien:
- Peradangan atau gagal ginjal
Efek samping lainnya
Efek samping lain telah terjadi pada sejumlah kecil orang, tetapi frekuensi pastinya tidak diketahui:
- perasaan jarum dan pin
- rasa tidak enak di mulut
- menguningnya bagian putih mata atau kulit.
Efek samping lain yang mungkin muncul dalam tes darah adalah:
- penghancuran sel darah merah yang terlalu cepat
- peningkatan beberapa jenis sel darah putih
- penurunan jumlah sel darah putih yang parah.
Pelaporan efek samping
Jika Anda mendapatkan efek samping, bicarakan dengan dokter atau apoteker Anda, termasuk kemungkinan efek samping yang tidak tercantum dalam selebaran ini. Anda juga dapat melaporkan efek samping secara langsung melalui sistem pelaporan di: www.agenziafarmaco.it/it/responsabili Dengan melaporkan efek samping Anda dapat membantu memberikan informasi lebih lanjut tentang keamanan obat ini.
Kadaluwarsa dan Retensi
Jauhkan obat ini dari pandangan dan jangkauan anak-anak.
Jangan menggunakan obat ini setelah tanggal kadaluwarsa yang tertera pada vial dan karton luar setelah tanggal kadaluwarsa. Tanggal kedaluwarsa mengacu pada hari terakhir bulan itu. Simpan di bawah 25 ° C.
Solusi yang dilarutkan
Dokter, apoteker, atau perawat Anda akan menyiapkan obat dalam air untuk injeksi atau cairan yang kompatibel. Setelah disiapkan, obat harus digunakan dalam waktu 6 hari jika disimpan di lemari es (pada suhu 4 ° C) atau dalam waktu 9 jam jika disimpan pada suhu 4 ° C. suhu lingkungan (di bawah 25? C).
Simpan vial dalam karton aslinya untuk melindunginya dari cahaya.
Jangan membuang obat apa pun melalui air limbah atau limbah rumah tangga. Tanyakan apoteker Anda bagaimana cara membuang obat yang sudah tidak digunakan lagi. Ini akan membantu melindungi lingkungan.
Informasi lainnya
Apa isi Starcef?
- Starcef tersedia dalam kekuatan berikut: 250mg / 1ml, 500mg / 1.5ml dan 1g / 3ml. Zat aktifnya adalah ceftazidime (hadir sebagai ceftazidime pentahydrate).
Starcef 250 mg / 1 ml bubuk dan pelarut untuk larutan injeksi mengandung 250 mg ceftazidime
Starcef 500 mg / 1,5 ml bubuk dan pelarut untuk larutan injeksi mengandung 500 mg ceftazidime
Starcef 1 g / 3 ml bubuk dan pelarut untuk larutan injeksi mengandung 1 g ceftazidime
- Satu-satunya komponen lainnya adalah natrium karbonat (steril anhidrat).
- Lihat bagian 2 untuk informasi penting lainnya tentang natrium, salah satu komponen Starcef.
Seperti apa rupa Starcef dan isi paketnya
Starcef 250 mg / 1 ml bubuk dan pelarut untuk larutan injeksi:
- 1 botol bubuk putih hingga krim steril 250 mg, terkandung dalam botol kaca 17 ml dengan sumbat karet bromobutil dan segel aluminium flip-off + 1 botol pelarut dari 1 ml kaca
Starcef 500 mg / 1,5 ml bubuk dan pelarut untuk larutan injeksi:
- 1 botol bubuk berwarna putih hingga krem steril 500 mg, terkandung dalam botol kaca 17 ml dengan sumbat karet bromobutil dan segel aluminium flip-off + 1 botol pelarut 1,5 ml kaca
Starcef 1 g / 3 ml bubuk dan pelarut untuk larutan injeksi:
- 1 botol bubuk berwarna putih hingga krem steril 1 g, terkandung dalam botol kaca 17 ml dengan sumbat karet bromobutil dan segel aluminium flip-off + 1 botol pelarut 3 ml kaca
Dokter, apoteker, atau perawat Anda akan menyiapkan injeksi atau infus dalam air untuk injeksi atau cairan infus yang sesuai. Setelah disiapkan, Stacef berubah warna dari kuning muda menjadi kuning. Ini sangat normal.
Sumber Paket Leaflet: AIFA (Badan Obat Italia). Konten yang diterbitkan pada Januari 2016. Informasi yang ada mungkin tidak up-to-date.
Untuk memiliki akses ke versi terbaru, disarankan untuk mengakses situs web AIFA (Badan Obat Italia). Penafian dan informasi yang berguna.
01.0 NAMA PRODUK OBAT
STARCEF POWDER DAN SOLVENT UNTUK SOLUSI INJEKSI
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF
Starcef 250 mg / 1 ml bubuk dan pelarut untuk larutan injeksi
Setiap vial mengandung 250 mg ceftazidime (sebagai pentahidrat) dengan natrium karbonat (118 mg per gram ceftazidime).
Eksipien dengan efek yang diketahui
Setiap vial mengandung 13 mg (0,58 mmol) sodium per vial.
Starcef 500 mg / 1,5 ml bubuk dan pelarut untuk larutan injeksi
Setiap vial mengandung 500 mg ceftazidime (sebagai pentahidrat) dengan natrium karbonat (118 mg per gram ceftazidime).
Eksipien dengan efek yang diketahui
Setiap vial mengandung 26 mg (1,15 mmol) sodium per vial.
Starcef 1 g / 3 ml bubuk dan pelarut untuk larutan injeksi
Setiap vial mengandung 1 g ceftazidime (sebagai pentahidrat) dengan natrium karbonat (118 mg per gram ceftazidime).
Eksipien dengan efek yang diketahui
Setiap vial mengandung 52 mg (2,3 mmol) sodium per vial.
Untuk daftar lengkap eksipien, lihat bagian 6.1.
03.0 FORMULIR FARMASI
250 mg / 1 ml bubuk dan pelarut untuk larutan injeksi
Bubuk untuk solusi untuk injeksi
Botol berisi bubuk putih steril hingga krim.
1 ml botol pelarut kaca tak berwarna tipe I.
500 mg / 1,5 ml bubuk dan pelarut untuk larutan injeksi
Bubuk untuk solusi untuk injeksi
Botol berisi bubuk putih steril hingga krim.
Tipe I botol pelarut kaca tak berwarna 1,5 ml.
1 g / 3 ml bubuk dan pelarut untuk larutan injeksi
Bubuk untuk solusi untuk injeksi
Botol berisi bubuk putih steril hingga krim.
Tipe I kaca tak berwarna vial pelarut 3 ml.
04.0 INFORMASI KLINIS
04.1 Indikasi Terapi
Starcef diindikasikan untuk pengobatan infeksi yang tercantum di bawah ini pada orang dewasa dan anak-anak termasuk neonatus (sejak lahir).
• Pneumonia nosokomial
• Infeksi bronkopulmoner pada fibrosis kistik
• Bakteri meningitis
• Otitis media supuratif kronis
• Otitis eksterna maligna
• Infeksi saluran kemih dengan komplikasi
• Infeksi kulit dan jaringan lunak yang rumit
• Infeksi intra-abdomen yang rumit
• Infeksi tulang dan sendi
• Peritonitis terkait dialisis pada pasien dengan dialisis peritoneal rawat jalan berkelanjutan (Dialisis peritoneal rawat jalan berkelanjutan-CAPD).
Pengobatan pasien dengan bakteremia yang terjadi atau diduga terkait dengan salah satu infeksi yang tercantum di atas.
Ceftazidime dapat digunakan dalam pengelolaan pasien neutropenia dengan demam yang diduga disebabkan oleh "infeksi bakteri".
Ceftazidime dapat digunakan dalam profilaksis perioperatif infeksi saluran kemih pasien yang menjalani reseksi prostat trans-uretra (reseksi trans-uretra prostat-TURP).
Pilihan ceftazidime harus memperhitungkan spektrum antibakterinya yang terbatas terutama pada bakteri aerob Gram negatif (lihat bagian 4.4 dan 5.1).
Ceftazidime harus diberikan bersama dengan agen antibakteri lain setiap kali bakteri yang dianggap berpotensi bertanggung jawab untuk infeksi berada di luar spektrum aktivitasnya.
Pedoman resmi tentang penggunaan yang tepat dari agen antibakteri harus dipertimbangkan.
04.2 Posologi dan cara pemberian
Dosis
Tabel 1: dewasa dan anak-anak 40 kg
Tabel 2: anak-anak
Populasi pediatrik
Keamanan dan kemanjuran Starcef yang diberikan sebagai infus kontinu pada bayi dan anak-anak berusia 2 bulan belum ditetapkan.
Warga senior
Mengingat penurunan klirens ceftazidime terkait usia pada pasien usia lanjut, dosis harian biasanya tidak boleh melebihi 3 g pada pasien di atas usia 80 tahun.
Insufisiensi hati
Data yang tersedia tidak menunjukkan perlunya penyesuaian dosis untuk pasien dengan gangguan hati ringan sampai sedang. Tidak ada data dari penelitian pada pasien dengan gangguan hati berat (lihat juga bagian 5.2). Pemantauan klinis yang ketat untuk keamanan dan kemanjuran disarankan.
Gagal ginjal
Ceftazidime diekskresikan tidak berubah oleh ginjal. Oleh karena itu, pada pasien dengan gangguan fungsi ginjal dosis harus dikurangi (lihat juga bagian 4.4).
Dosis awal 1 g harus diberikan. Dosis pemeliharaan harus didasarkan pada klirens kreatinin:
Tabel 3: Dosis pemeliharaan Starcef yang direkomendasikan pada insufisiensi ginjal - infus intermiten
Dewasa dan anak-anak ≥ 40 kg
Pada pasien dengan infeksi berat dosis unit harus ditingkatkan 50% atau frekuensi dosis ditingkatkan.
Pada anak-anak, perkiraan bersihan kreatinin harus dihitung sebagai fungsi dari luas permukaan tubuh atau massa tubuh tanpa lemak.
Anak-anak
Pemantauan klinis yang ketat untuk keamanan dan kemanjuran disarankan.
Tabel 4: Dosis pemeliharaan Starcef yang direkomendasikan pada insufisiensi ginjal - infus berkelanjutan
Dewasa dan anak-anak 40 kg
Perhatian disarankan dalam pemilihan dosis. Pemantauan klinis yang ketat untuk keamanan dan kemanjuran disarankan.
Anak-anak
Keamanan dan kemanjuran Starcef diberikan sebagai infus berkelanjutan pada anak-anak dengan berat badan
Jika infus kontinu digunakan pada anak dengan insufisiensi ginjal, klirens kreatinin harus dihitung sebagai fungsi luas permukaan tubuh atau massa tubuh tanpa lemak.
Hemodialisis
Nilai paruh serum selama hemodialisis berkisar antara 3 hingga 5 jam.
Setelah setiap periode hemodialisis, dosis pemeliharaan ceftazidime yang direkomendasikan pada Tabel 5 dan 6 harus diulang.
Dialisis peritoneal
Ceftazidime dapat digunakan dalam dialisis peritoneal dan dialisis peritoneal rawat jalan terus menerus (CAPD).
Selain penggunaan intravena, ceftazidime dapat ditambahkan ke cairan dialisis (biasanya 125 hingga 250 mg per 2 liter larutan dialisis).
Untuk pasien dengan insufisiensi ginjal pada hemodialisis arteriovenosa kontinu atau hemofiltrasi aliran tinggi di unit perawatan intensif: 1 g per hari baik sebagai dosis tunggal atau dalam dosis terbagi. Untuk hemofiltrasi aliran rendah, ikuti dosis yang dianjurkan pada insufisiensi ginjal.
Untuk pasien hemofiltrasi veno-vena dan hemodialisis veno-vena, ikuti dosis yang dianjurkan pada Tabel 5 dan 6 di bawah ini.
Tabel 5: Pedoman dosis hemofiltrasi vena-vena berkelanjutan
Tabel 6: Pedoman dosis hemodialisis vena-vena berkelanjutan
p> Cara pemberian
Dosis tergantung pada tingkat keparahan, sensitivitas, lokasi dan jenis infeksi serta usia dan fungsi ginjal pasien.
Starcef 500 mg dan 250 mg harus diberikan melalui injeksi intravena atau injeksi intramuskular dalam. Tempat injeksi intramuskular yang direkomendasikan adalah kuadran atas luar gluteus maximus atau bagian lateral paha. Solusi Starcef dapat diberikan langsung ke pembuluh darah. Rute standar pemberian yang direkomendasikan adalah dengan injeksi intravena intermiten. Pemberian intramuskular hanya boleh dipertimbangkan bila rute pemberian intravena tidak memungkinkan atau kurang tepat untuk pasien. Starcef 1 g harus diberikan melalui injeksi intravena atau infus atau injeksi intramuskular dalam. Tempat injeksi intramuskular yang direkomendasikan adalah kuadran atas luar gluteus maximus atau bagian lateral paha. Larutan Starcef dapat diberikan langsung ke dalam vena atau dimasukkan melalui set infus jika pasien menerima cairan melalui suntikan.
Rute pemberian standar yang direkomendasikan adalah dengan injeksi intravena intermiten atau infus intravena terus menerus). Pemberian intramuskular hanya boleh dipertimbangkan bila rute pemberian intravena tidak memungkinkan atau kurang tepat untuk pasien.
04.3 Kontraindikasi
Hipersensitivitas terhadap ceftazidime, sefalosporin lain atau salah satu eksipien yang tercantum di bagian 6.1.
Riwayat hipersensitivitas berat (misalnya reaksi anafilaksis) terhadap jenis agen antibakteri beta-laktam lainnya (penisilin, monobaktam, dan karbapenem).
04.4 Peringatan khusus dan tindakan pencegahan yang tepat untuk digunakan
Hipersensitivitas
Seperti semua agen antibakteri beta-laktam, reaksi hipersensitivitas yang parah dan terkadang fatal telah dilaporkan. Jika terjadi reaksi hipersensitivitas yang parah, pengobatan dengan ceftazidime harus segera dihentikan dan tindakan darurat yang tepat harus dilakukan.
Sebelum memulai pengobatan, harus dipastikan bahwa pasien tidak memiliki riwayat reaksi hipersensitivitas yang parah terhadap ceftazidime atau sefalosporin lain atau jenis agen beta-laktam lainnya. Perhatian khusus harus dilakukan jika ceftazidime diberikan kepada pasien dengan riwayat hipersensitivitas non-berat terhadap agen beta-laktam lainnya.
Spektrum aktivitas
Ceftazidime memiliki spektrum aktivitas antibakteri yang terbatas. Hal ini tidak cocok untuk digunakan sebagai agen antibakteri tunggal untuk pengobatan jenis infeksi tertentu kecuali patogen telah didokumentasikan dan diketahui sensitif atau ada kecurigaan tinggi bahwa patogen yang paling mungkin sensitif pengobatan dengan ceftazidime. berlaku terutama ketika mempertimbangkan pengobatan pasien dengan bakteremia dan ketika mengobati meningitis bakteri, infeksi kulit dan jaringan lunak, dan infeksi tulang dan sendi. Selanjutnya, ceftazidime sensitif terhadap hidrolisis beberapa beta laktamase spektrum luas.beta-laktamase spektrum luas-ESBL).
Oleh karena itu informasi tentang prevalensi organisme penghasil ESBL harus dipertimbangkan ketika memilih pengobatan ceftazidine.
Kolitis pseudomembran
Kolitis yang berhubungan dengan agen antibakteri dan kolitis pseudo-membran telah dilaporkan terjadi pada hampir semua agen antibakteri, termasuk ceftazidime dan dapat berkisar dari ringan hingga mengancam jiwa. Oleh karena itu, penting untuk mempertimbangkan diagnosis ini pada pasien yang datang dengan diare selama atau setelah pemberian ceftazidime (lihat bagian 4.8). Penghentian terapi ceftazidime dan pemberian pengobatan khusus untuk Clostridium difficile harus diperhitungkan. Produk obat yang menghambat peristaltik tidak boleh diberikan.
Fungsi ginjal
Pengobatan bersamaan dengan sefalosporin dosis tinggi dan produk obat nefrotoksik seperti aminoglikosida atau diuretik kuat (misalnya furosemide) mungkin memiliki efek buruk pada fungsi ginjal.
Ceftazidime dieliminasi oleh ginjal, oleh karena itu dosis harus dikurangi sesuai dengan derajat kerusakan ginjal. Pasien dengan insufisiensi ginjal harus dipantau secara hati-hati untuk efikasi dan keamanan.Sekuele neurologis kadang-kadang dilaporkan ketika dosis belum dikurangi pada pasien dengan insufisiensi ginjal (lihat bagian 4.2 dan 4.8).
Pertumbuhan berlebih dari mikroorganisme yang tidak sensitif
Penggunaan jangka panjang dapat menyebabkan pertumbuhan berlebih dari mikroorganisme yang tidak sensitif (misalnya Enterococci, jamur) yang mungkin memerlukan penghentian pengobatan atau tindakan lain yang sesuai. Pemantauan berulang terhadap kondisi pasien sangat penting.
Interaksi dengan tes / tes
Ceftazidime tidak mengganggu tes enzimatik untuk penentuan glikosuria, tetapi sedikit gangguan (positif palsu) dapat terjadi dengan metode berdasarkan reduksi tembaga (Benedict, Fehling, Clinitest).
Ceftazidime tidak mengganggu uji alkaline picrate untuk penentuan kreatinin. Perkembangan tes Coombs positif yang terkait dengan penggunaan ceftazidime pada sekitar 5% pasien dapat mengganggu tes kompatibilitas darah.
Kandungan natrium
Informasi penting tentang eksipien Starcef:
250 mg / 1 ml bubuk dan pelarut untuk larutan injeksi
Starcef 250 mg mengandung 13 mg (0,58 mmol) sodium per vial.
500 mg / 1,5 ml bubuk dan pelarut untuk larutan injeksi
Starcef 500 mg mengandung 26 mg (1,15 mmol) sodium per vial.
1 g / 3 ml bubuk dan pelarut untuk larutan injeksi
Starcef 1 g mengandung 52 mg (2,3 mmol) sodium per vial.
Ini harus dipertimbangkan untuk pasien yang menjalani diet natrium terkontrol.
04.5 Interaksi dengan produk obat lain dan bentuk interaksi lainnya
Hanya studi interaksi dengan probenesid dan furosemide yang telah dilakukan.
Penggunaan bersama dosis tinggi dengan produk obat nefrotoksik mungkin memiliki efek buruk pada fungsi ginjal (lihat bagian 4.4).
Kloramfenikol merupakan antagonis in vitro ceftazidime dan sefalosporin lainnya. Relevansi klinis dari pengamatan ini tidak diketahui, tetapi jika pemberian ceftazidime dan kloramfenikol secara bersamaan diusulkan, kemungkinan antagonisme antara kedua antibiotik harus dipertimbangkan.
04.6 Kehamilan dan menyusui
Kehamilan
Ada sejumlah terbatas data tentang penggunaan ceftazidime pada wanita hamil.
Penelitian pada hewan tidak menunjukkan efek berbahaya langsung atau tidak langsung sehubungan dengan kehamilan, perkembangan embrio / janin, persalinan atau perkembangan pascakelahiran (lihat bagian 5.3).
Starcef hanya boleh diresepkan untuk wanita hamil jika manfaatnya lebih besar daripada risikonya.
Waktunya memberi makan
Ceftazidime diekskresikan dalam ASI dalam jumlah kecil tetapi pada dosis terapeutik ceftazidime tidak ada efek pada bayi yang disusui. Ceftazidime dapat digunakan selama menyusui.
Kesuburan
Tidak ada data yang tersedia.
04.7 Efek pada kemampuan mengemudi dan menggunakan mesin
Studi tentang kemampuan mengemudi dan menggunakan mesin belum dilakukan.Namun, efek yang tidak diinginkan (misalnya pusing) dapat terjadi yang dapat mengganggu kemampuan mengemudi atau menggunakan mesin (lihat bagian 4.8).
04.8 Efek yang tidak diinginkan
Efek samping yang paling umum adalah eosinofilia, trombositosis, flebitis atau tromboflebitis dengan pemberian intravena, diare, peningkatan sementara enzim hati, ruam makulopapular atau urtikaria, nyeri dan / atau peradangan setelah injeksi intramuskular, dan tes Coombs positif.
Data dari uji klinis yang disponsori dan tidak disponsori digunakan untuk menentukan frekuensi efek samping yang umum dan tidak umum. Frekuensi yang ditetapkan untuk semua efek yang tidak diinginkan lainnya ditentukan terutama berdasarkan data farmakovigilans pasca-pemasaran dan mengacu pada frekuensi pelaporan daripada frekuensi sebenarnya.Dalam setiap kelas frekuensi, efek yang tidak diinginkan dilaporkan dalam urutan keparahan yang menurun. Konvensi berikut digunakan untuk klasifikasi frekuensi:
Sangat umum (≥ 1/10)
Umum (≥1 / 100 tahun
Jarang (≥1 / 1000 tahun
Langka (≥1 / 10.000 tahun
Sangat langka (
Tidak diketahui (tidak dapat diperkirakan dari data yang tersedia)
1 Ada laporan gejala sisa neurologis termasuk tremor, mioklonus, kejang, ensefalopati dan koma pada pasien dengan insufisiensi ginjal di mana dosis Starcef tidak cukup dikurangi.
2 Diare dan kolitis mungkin berhubungan dengan adanya Clostridium difficile dan hadir dalam bentuk kolitis pseudomembran.
3ALT (SGPT), AST (SOGT), LHD, GGT, alkaline phosphatase.
4 Ada kasus yang jarang terjadi di mana DRESS telah dikaitkan dengan ceftazidime.
5 Tes Coombs positif berkembang pada sekitar 5% pasien dan dapat mengganggu tes kompatibilitas darah.
Pelaporan dugaan reaksi merugikan
Pelaporan dugaan reaksi merugikan yang terjadi setelah otorisasi produk obat penting karena memungkinkan pemantauan berkelanjutan dari keseimbangan manfaat / risiko produk obat. Profesional kesehatan diminta untuk melaporkan setiap dugaan reaksi merugikan melalui sistem pelaporan nasional. "alamat: http ://www.agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosis
Overdosis dapat menyebabkan gejala sisa neurologis termasuk ensefalopati, kejang dan koma.
Gejala overdosis dapat terjadi jika dosis tidak dikurangi dengan tepat pada pasien dengan insufisiensi ginjal (lihat bagian 4.2 dan 4.4).
Kadar serum ceftazidime dapat dikurangi dengan hemodialisis atau dialisis peritoneal.
05.0 SIFAT FARMAKOLOGIS
05.1 Sifat farmakodinamik
Kelompok farmakoterapi: Antibakteri untuk penggunaan sistemik. Sefalosporin generasi ketiga - kode ATC: J01DD02.
Mekanisme aksi
Ceftazidime menghambat sintesis dinding sel bakteri setelah adhesi ke protein pengikat penisilin.Protein pengikat penisilin -PBP). Ini melibatkan gangguan biosintesis dinding sel (peptidoglikan) yang menyebabkan lisis dan kematian sel bakteri.
Hubungan farmakokinetik / farmakodinamik
Untuk sefalosporin, indeks farmakokinetik-farmakodinamik yang paling penting berkorelasi dengan kemanjuran in vivo telah terbukti sebagai persentase waktu dalam rentang dosis di mana konsentrasi obat yang tidak terikat protein tetap berada di atas konsentrasi hambat minimum (KHM) ceftazidime untuk spesies bakteri target individu (yaitu T% > MIC).
Mekanisme resistensi
Resistensi bakteri terhadap ceftazidime mungkin disebabkan oleh satu atau lebih mekanisme berikut:
• hidrolisis oleh beta laktamase. Ceftazidime dapat dihidrolisis secara efektif oleh beta-laktamase spektrum luas (beta-laktamase spektrum luas-ESBLs) termasuk keluarga SHV dari ESBLs dan enzim AmpC yang dapat diinduksi atau ditekan secara stabil pada beberapa spesies bakteri Gram-negatif aerobik
• penurunan afinitas protein pengikat penisilin untuk ceftazidime
• impermeabilitas membran luar yang membatasi akses ceftazidime ke protein pengikat penisilin pada organisme Gram-negatif
• pompa penghabisan bakteri.
Breakpoint
Titik henti Konsentrasi Penghambatan Minimum (Minimum Inhibitory Concentration (MIC)) yang ditetapkan oleh Komite Eropa untuk Tes Sensitivitas Antibakteri (Komite Eropa untuk Pengujian Kerentanan Antimikroba - EUCAST) adalah sebagai berikut:
S = sensitif, I = menengah, R = resisten.
1 Breakpoints terkait dengan terapi dosis tinggi (2 g x 3).
2 Titik putus terkait non-spesies sebagian besar ditentukan berdasarkan data PK / PD dan tidak bergantung pada distribusi MIC spesies tertentu. Mereka hanya digunakan untuk spesies yang tidak disebutkan dalam tabel atau catatan di bawah.
Sensitivitas mikrobiologis
Prevalensi resistensi yang didapat dapat bervariasi secara geografis dan dengan waktu untuk spesies yang dipilih, dan informasi lokal tentang resistensi diinginkan, terutama ketika mengobati infeksi berat. Jika perlu, ketika prevalensi resistensi lokal sedemikian rupa sehingga kegunaan ceftazidime pada beberapa jenis infeksi dipertanyakan, saran ahli harus dicari.
Spesies yang umumnya sensitif
aerob gram positif:
Streptococcus pyogenes
Streptococcus agalactiae
aerob gram negatif:
Citrobacter koseri
Haemophilus influenzae
Moraxella catarrhalis
Neisseria meningitidis
Pasteurella multocida
Proteus mirabilis
Proteus sp. (yang lain)
Providencia sp.
Spesies yang staminanya bisa menjadi masalah
aerob gram negatif:
Acinetobacter baumanii £+
Burkholderia cepacia
Citrobacter freundii
Enterobacter aerogenes
Enterobacter cloacae
Escherichia coli
Klebsiella pneumoniae
Klebsiella sp. (yang lain)
Pseudomonas aeruginosa
serratia sp.
Morganella morganii
aerob gram positif:
Stafilokokus aureus £
Streptokokus pneumonitis ££
Streptokokus grup viridans
Bakteri anaerob gram positif:
Clostridium perfringens
Peptostreptokokus sp.
Bakteri anaerob gram negatif:
Fusobacterium sp.
Organisme yang resisten secara inheren
aerob gram positif:
Enterokokus spp. termasuk Enterococcus faecalis dan Enterococcus faecium
Listeria sp.
Bakteri anaerob gram positif:
Clostridium difficile
Bakteri anaerob gram negatif:
Bacteroides sp. (banyak spesies Bacteroides fragilis tahan).
Yang lain:
Klamidia sp.
mikoplasma sp.
Legionella sp.
£S. aureus yang sensitif terhadap methicillin dianggap memiliki sensitivitas yang rendah terhadap ceftazidime. Semua S. aureus resisten methicillin resisten terhadap ceftazidime.
££S. pneumoniae yang menunjukkan kerentanan menengah atau resisten terhadap penisilin dapat diharapkan menunjukkan setidaknya penurunan kerentanan terhadap ceftazidime.
+Tingkat resistensi yang tinggi telah diamati di satu atau lebih wilayah / negara / wilayah di dalam Uni Eropa.
05.2 Sifat farmakokinetik
Penyerapan
Setelah pemberian intramuskular 500 mg dan 1 g ceftazidime, kadar plasma puncak masing-masing 18 dan 37 mg / l, dicapai dengan cepat. Lima menit setelah pemberian bolus intravena 500 mg, 1 g atau 2 g, kadar plasma masing-masing adalah 46, 87 dan 170 mg / l. Kinetika ceftazidime linier dalam kisaran dosis tunggal 0,5 sampai 2 g setelah pemberian intravena atau intramuskular.
Distribusi
Pengikatan protein serum ceftazidime rendah dan sekitar 10%. Konsentrasi yang melebihi MIC untuk patogen umum dapat diperoleh di jaringan seperti tulang, jantung, empedu, sputum, aqueous humor, cairan sinovial, pleura dan peritoneal Ceftazidime dengan cepat melintasi plasenta dan diekskresikan dalam ASI Penetrasi ke dalam darah utuh sawar otak yang buruk mengakibatkan rendahnya kadar ceftazidime di CSF tanpa adanya peradangan.Namun, konsentrasi 4 sampai 20 mg / l atau lebih ditemukan di CSF ketika meningen meradang.
Biotransformasi
Ceftazidime tidak dimetabolisme.
Eliminasi
Setelah pemberian parenteral, kadar plasma menurun dengan waktu paruh sekitar 2 jam Ceftazidime diekskresikan tidak berubah dalam urin melalui filtrasi glomerulus. Sekitar 80-90% dari dosis ditemukan dalam urin dalam waktu 24 jam, kurang dari 1% diekskresikan melalui empedu.
Populasi pasien khusus
Gagal ginjal
Eliminasi ceftazidime menurun pada pasien dengan gangguan fungsi ginjal dan dosis harus dikurangi (lihat bagian 4.2).
Insufisiensi hati
Adanya disfungsi hati ringan sampai sedang tidak berpengaruh pada farmakokinetik ceftazidime dalam dosis individu 2 g intravena setiap 8 jam selama 5 hari asalkan fungsi ginjal tidak terganggu (lihat bagian 4.2).
Warga senior
Penurunan klirens yang diamati pada pasien usia lanjut terutama disebabkan oleh penurunan klirens ceftazidime terkait usia.Rata-rata waktu paruh eliminasi berkisar antara 3,5 hingga 4 jam setelah dosis tunggal atau berulang selama 7 hari dua kali sehari, 2 g dengan bolus intravena injeksi pada pasien lanjut usia berusia 80 tahun atau lebih.
Populasi pediatrik
Waktu paruh ceftazidime memanjang pada bayi prematur dan bayi cukup bulan dari 4,5 hingga 7,5 jam setelah dosis 25 hingga 30 mg / kg. Namun, pada usia 2 bulan, waktu paruh berada dalam nilai untuk orang dewasa. .
05.3 Data keamanan praklinis
Data non-klinis mengungkapkan tidak ada bahaya khusus bagi manusia berdasarkan studi konvensional farmakologi keselamatan, toksisitas dosis berulang, genotoksisitas, toksisitas reproduksi. Studi karsinogenisitas belum dilakukan dengan ceftazidime.
06.0 INFORMASI FARMASI
06.1 Eksipien
Botol bubuk: natrium karbonat (steril anhidrat).
Ampul pelarut: air untuk injeksi.
06.2 Ketidakcocokan
Starcef dalam larutan natrium bikarbonat untuk injeksi kurang stabil dibandingkan cairan lain untuk pemberian intravena. Solusi ini tidak disarankan untuk pengenceran. Starcef tidak boleh dicampur dalam set infus atau jarum suntik yang sama dengan aminoglikosida.
Pembentukan endapan telah dilaporkan dengan menambahkan vankomisin ke dalam larutan ceftazidime.
Oleh karena itu, disarankan untuk membiarkan jumlah cairan yang cukup mengalir ke dalam set infus dan jalur infus di antara kedua pemberian.
06.3 Masa berlaku
3 tahun
Setelah rekonstitusi
Stabilitas kimia dan fisik dalam penggunaan telah ditunjukkan selama 6 hari pada 4 ° C dan 9 jam pada 25 ° C. Dari sudut pandang mikrobiologi, larutan yang dilarutkan harus segera digunakan. Jika tidak segera digunakan, waktu dan kondisi penyimpanan yang digunakan sebelum digunakan adalah tanggung jawab pengguna dan biasanya tidak lebih dari 24 jam pada 2-8 ° C, kecuali rekonstitusi telah dilakukan dalam kondisi aseptik, diperiksa dan divalidasi.
Setelah pengenceran
Stabilitas kimia dan fisik dalam penggunaan telah ditunjukkan selama 6 hari pada 4 ° C dan 9 jam pada 25 ° C.
Dari sudut pandang mikrobiologi, larutan yang dilarutkan dan diencerkan harus segera digunakan. Jika tidak segera digunakan, waktu dan kondisi penyimpanan yang digunakan sebelum digunakan adalah tanggung jawab pengguna dan biasanya tidak akan lebih lama dari 24 jam pada 2-8 ° C, kecuali rekonstitusi telah dilakukan dalam kondisi aseptik, diperiksa dan divalidasi.
06.4 Tindakan pencegahan khusus untuk penyimpanan
Simpan di bawah 25 ° C.
Simpan vial di karton luar untuk melindungi dari cahaya.
Untuk kondisi penyimpanan setelah rekonstitusi lihat bagian 6.3.
06.5 Sifat kemasan langsung dan isi kemasan
Starcef 250 mg / 1 ml bubuk dan pelarut untuk larutan injeksi: - 1 botol bubuk 250 mg dalam gelas tidak berwarna Ph.Eur.Type III 17 ml dengan sumbat karet bromobutil dan segel aluminium flip-off + 1 ampul pelarut 1 ml dalam gelas tipe I yang tidak berwarna
Starcef 500 mg / 1,5 ml bubuk dan pelarut untuk larutan injeksi:
- 1 botol bubuk 500 mg dalam kaca tak berwarna Ph.Eur.Tipe III 17 ml dengan sumbat karet bromobutil dan segel aluminium flip-off + 1 botol pelarut 1,5 ml dalam kaca tak berwarna tipe I
Starcef 1 g / 3 ml bubuk dan pelarut untuk larutan injeksi:
- 1 botol bubuk 1 g dalam kaca tak berwarna Ph.Eur.Tipe III 17 ml dengan sumbat karet bromobutil dan segel aluminium flip-off + 1 botol pelarut 3 ml dalam kaca tak berwarna tipe I
06.6 Petunjuk penggunaan dan penanganan
Semua jenis botol Starcef disuplai di bawah tekanan yang dikurangi. Saat produk larut, karbon dioksida dilepaskan dan tekanan positif berkembang. Gelembung kecil karbon dioksida dalam larutan yang dilarutkan dapat diabaikan.
Instruksi untuk rekonstitusi
Lihat tabel untuk penambahan volume dan konsentrasi larutan yang mungkin berguna jika dosis fraksional diperlukan.
* Catatan: Volume larutan ceftazidime yang dihasilkan dalam media rekonstitusi meningkat karena faktor perpindahan obat yang menghasilkan konsentrasi yang tercantum dalam mg / ml yang ditunjukkan pada tabel di atas.
Warna larutan dapat bervariasi dari kuning pucat hingga kuning, tergantung pada konsentrasi, jenis pengencer, dan kondisi penyimpanan yang digunakan. Dalam kerangka rekomendasi yang ditetapkan, aktivitas produk tidak terpengaruh oleh variasi warna tersebut. Ceftazidime pada konsentrasi antara 1 mg / ml dan 40 mg / ml kompatibel dengan:
• natrium klorida 9 mg / ml (0,9%) untuk injeksi
• natrium laktat M / 6 untuk injeksi
• senyawa natrium laktat untuk injeksi (larutan Hartmann)
• Dekstrosa 5% untuk injeksi
• 0,225% natrium klorida dan 5% dekstrosa untuk injeksi
• 0,45% natrium klorida dan 5% dekstrosa untuk injeksi
• Natrium klorida 0,9% dan dekstrosa 5% untuk injeksi
• 0,18% natrium klorida dan 4% dekstrosa untuk injeksi
• Dekstrosa 10% untuk injeksi
• Dextran 40 10% untuk injeksi dalam 0,9% natrium klorida untuk injeksi
• Dextran 40 10% untuk injeksi dalam 5% dekstrosa untuk injeksi
• Dextran 70 6% untuk injeksi dalam 0,9% natrium klorida untuk injeksi
• Dextran 70 6% untuk injeksi dalam dekstrosa 5% untuk injeksi
Ceftazidime pada konsentrasi mulai dari 0,05 mg / ml hingga 0,25 mg / ml kompatibel dengan larutan laktat untuk dialisis intra-peritoneal.
Ceftazidime pada konsentrasi yang tercantum dalam tabel di atas dapat dilarutkan untuk penggunaan intramuskular dengan 0,5% atau 1% lidokain hidroklorida untuk injeksi.
Isi botol 500 mg ceftazidime untuk injeksi, dilarutkan dengan 1,5 ml air untuk injeksi, dapat ditambahkan ke larutan metronidazol (500 mg dalam 100 ml) dan keduanya mempertahankan aktivitasnya.
250 mg, 500 mg 1 g bubuk untuk larutan injeksi
Persiapan untuk solusi injeksi bolus
1. Masukkan jarum semprit melalui penutup vial dan masukkan jumlah pengencer yang disarankan. Tidak adanya udara dapat memudahkan masuknya pengencer. Lepaskan jarum semprit.
2. Kocok untuk melarutkan: Karbon dioksida dilepaskan dan larutan bening akan diperoleh dalam 1-2 menit.
3. Putar botolnya. Dengan plunger spuit diturunkan sepenuhnya, masukkan jarum melalui lubang vial dan tarik volume total larutan ke dalam spuit (tekanan dalam vial dapat membantu aspirasi). Pastikan jarum tetap berada di dalam larutan dan tidak masuk ke ruang atas. Larutan yang disedot mungkin mengandung gelembung kecil karbon dioksida, ini dapat diabaikan.
Solusi ini dapat diberikan langsung ke dalam vena atau dimasukkan melalui infus jika pasien menerima cairan parenteral. Ceftazidime kompatibel dengan cairan infus bekas yang tercantum di atas.
Setiap larutan antibiotik yang tersisa harus dibuang.
Untuk sekali pakai saja.
Obat yang tidak terpakai dan limbah yang berasal dari obat ini harus dibuang sesuai dengan peraturan setempat.
07.0 PEMEGANG OTORITAS PEMASARAN
TANDA TANGAN. Spa. - Via di Scandicci, 37 - Florence.
08.0 NOMOR OTORITAS PEMASARAN
STARCEF 250 mg / 1 ml Bubuk dan pelarut untuk larutan injeksi "1 vial bubuk + 1 vial 1 ml pelarut" A.I.C .: 025859012
STARCEF 500 mg / 1,5 ml Bubuk dan pelarut untuk larutan injeksi "1 vial bubuk + 1 vial pelarut 1,5 ml" A.I.C .: 025859024
STARCEF 1 g / 3 ml Bubuk dan pelarut untuk larutan injeksi "1 botol bubuk + 1 botol 3 ml pelarut" A.I.C .: 025859036
09.0 TANGGAL OTORISASI PERTAMA ATAU PEMBARUAN KUASA
Tanggal otorisasi pertama: 6 Juli 1985
Tanggal pembaruan terakhir: Mei 2010
10.0 TANGGAL REVISI TEKS
September 2016