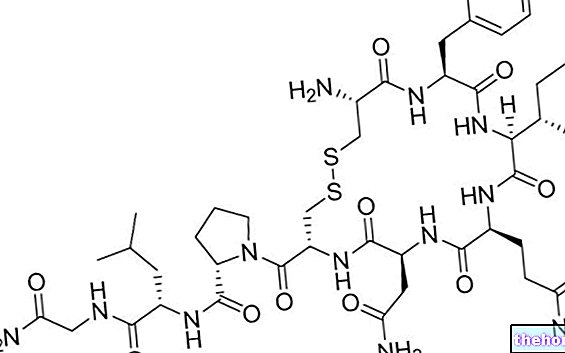
Untuk berbicara tentang dua puluh asam amino yang membentuk struktur protein dan yang dimodifikasi, perlu dijelaskan setidaknya dua belas jalur metabolisme khusus.
Tapi mengapa sel menggunakan begitu banyak jalur metabolisme yang membutuhkan energi (misalnya untuk meregenerasi situs katalitik enzim), masing-masing dengan warisan enzimatik, untuk mengkatabolisme asam amino? Dari hampir semua asam amino dimungkinkan untuk memperoleh, melalui jalur khusus, metabolit yang sebagian kecil digunakan untuk menghasilkan energi (misalnya, melalui glukoneogenesis dan jalur badan keton) tetapi yang terutama mengarah pada pembentukan kompleks molekul, dengan jumlah atom karbon yang tinggi (misalnya dari fenilalanin dan tirosin, hormon diproduksi di kelenjar adrenal yang khusus untuk tujuan ini); jika di satu sisi akan mudah untuk menghasilkan energi dari asam amino, di sisi lain akan rumit untuk membangun molekul kompleks mulai dari molekul kecil: katabolisme asam amino memungkinkan mereka untuk mengeksploitasi kerangka mereka untuk mendapatkan spesies yang lebih besar.
Dua atau tiga hektogram asam amino terdegradasi setiap hari oleh individu yang sehat: 60-100 g di antaranya berasal dari protein yang dimasukkan ke dalam makanan tetapi lebih dari 2 hektogram diperoleh dari pergantian normal protein yang merupakan bagian integral dari organisme ( asam amino dari protein ini, yang dirusak oleh proses redoks, digantikan oleh yang lain dan dikatabolisme).
Asam amino memberikan kontribusi energi dalam bentuk ATP: setelah menghilangkan gugus -amino, kerangka asam amino karbon yang tersisa, mengikuti transformasi yang sesuai, dapat memasuki siklus krebs. Selanjutnya, ketika suplai nutrisi kurang dan jumlah glukosa menurun, glukoneogenesis diaktifkan: asam amino glukoneogenetik dikatakan sebagai asam amino yang, setelah modifikasi yang tepat, dapat dimasukkan ke dalam glukoneogenesis; asam amino glukoneogenetik adalah asam amino yang dapat diubah menjadi piruvat atau dalam fumarat (fumarat dapat diubah menjadi malat yang meninggalkan mitokondria dan, di dalam sitoplasma, diubah menjadi oksaloasetat dari mana fosfoenol piruvat dapat diperoleh).
Yang baru saja dijelaskan adalah aspek yang sangat penting karena asam amino dapat memperbaiki kekurangan gula dalam kasus puasa segera; jika puasa berlanjut, setelah dua hari metabolisme lipid campur (karena struktur protein tidak dapat diserang terlalu banyak) pada fase inilah, karena glukoneogenesis sangat terbatas, asam lemak diubah menjadi asetil koenzim A dan badan keton . Dari puasa selanjutnya, otak juga beradaptasi untuk menggunakan badan keton.
Pemindahan gugus -amino dari asam amino terjadi melalui reaksi transaminasi; enzim yang mengkatalisis reaksi ini, mereka mengatakan, pada kenyataannya, transaminase (atau amino transferase). Enzim-enzim ini menggunakan kofaktor enzimatik yang disebut piridoksal fosfat, yang mengintervensi gugus aldehidanya. Pyridoxal phosphate adalah produk dari fosforilasi pyridoxine yang merupakan vitamin (B6) yang ditemukan terutama dalam sayuran.
Transaminase memiliki sifat sebagai berikut:
Spesifisitas tinggi untuk pasangan ketoglutarat-glutamat;
Mereka diberi nama setelah pasangan kedua.
Enzim transaminase selalu melibatkan pasangan ketoglutarat-glutamat dan dibedakan menurut pasangan kedua yang terlibat.
Contoh:
L"transaminase aspartat yaitu GOT (Glutamate-Ossal acetate Transaminase): enzim mentransfer gugus -amino dari aspartat ke -ketoglutarat, memperoleh oksaloasetat dan glutamat.
L"alanin transaminase yaitu GTP (Glutamate-Pyruvate Transaminase): enzim mentransfer gugus -amino dari "alanin ke" -ketoglutarat, memperoleh piruvat dan glutamat.
Berbagai transaminase menggunakan -ketoglurate sebagai akseptor gugus amino asam amino dan mengubahnya menjadi glutamat; sedangkan asam amino yang terbentuk digunakan dalam jalur badan keton.
Jenis reaksi ini dapat terjadi di kedua arah karena mereka memutuskan dan membentuk ikatan dengan kandungan energi yang sama.
Transaminase ada di sitoplasma dan di mitokondria (kebanyakan aktif di sitoplasma) dan berbeda dalam titik isoelektriknya.
Transaminase juga mampu mendekarboksilat asam amino.
Harus ada cara untuk mengubah glutamat kembali menjadi -ketoglutarat: ini dilakukan dengan deaminasi.
Di sana glutamat dehidrogenase itu adalah enzim yang mampu mengubah glutamat menjadi -ketoglutarat dan, oleh karena itu, mengubah gugus amino dari asam amino yang ditemukan dalam bentuk glutamat menjadi amonia. Apa yang terjadi adalah proses redoks yang melewati perantara -amino glutarat: amonia dan -ketoglutarat dilepaskan dan kembali ke sirkulasi.
Kemudian, pembuangan gugus amino dari asam amino melewati transaminase (yang berbeda menurut substratnya) dan glutamat dehidrogenase, yang menentukan pembentukan amonia.
Ada dua jenis glutamat dehidrogenase: sitoplasma dan mitokondria; kofaktor, yang juga merupakan kosubstrat enzim ini adalah NAD (P) +: glutamat dehidrogenase menggunakan NAD + atau NADP + sebagai akseptor daya pereduksi. Bentuk sitoplasma lebih suka, meskipun tidak eksklusif, NADP + sedangkan bentuk mitokondria lebih suka NAD +. Bentuk mitokondria memiliki tujuan untuk membuang gugus amino: ia mengarah pada pembentukan amonia (yang merupakan substrat untuk enzim khusus dalam mitokondria) dan NADH (yang dikirim ke rantai pernapasan). Bentuk sitoplasma bekerja dalam arah yang berlawanan yaitu, menggunakan amonia dan -ketoglutarat untuk memberikan glutamat (yang memiliki tujuan biosintesis): reaksi ini adalah biosintesis reduktif dan kofaktor yang digunakan adalah NADPH.
Glutamat dehidrogenase bekerja ketika diperlukan untuk membuang gugus amino dari asam amino seperti amonia (melalui urin) atau ketika kerangka asam amino diperlukan untuk menghasilkan energi: oleh karena itu enzim ini akan memiliki modulator negatif sistem yang merupakan indikasi ketersediaan energi yang baik (ATP, GTP dan NAD (P) H) dan sebagai modulator positif, sistem yang menunjukkan kebutuhan energi (AMP, ADP, GDP, NAD (P) +, asam amino dan hormon tiroid).
Asam amino (terutama leusin) adalah modulator positif glutamat dehidrogenase: jika asam amino ada di sitoplasma, asam amino dapat digunakan untuk sintesis protein, atau harus dibuang karena tidak dapat diakumulasikan (ini menjelaskan mengapa asam amino adalah modulator positif ) .
Pembuangan amonia: siklus urea
Ikan membuang amonia dengan memasukkannya ke dalam air melalui insang; burung mengubahnya menjadi asam urat (yang merupakan produk kondensasi) dan membuangnya dengan tinja. Mari kita lihat apa yang terjadi pada manusia: kita telah mengatakan bahwa glutamat dehidrogenase mengubah glutamat dalam - ketoglutarat dan amonia tetapi kami belum mengatakan bahwa ini hanya terjadi di mitokondria hati.
Peran mendasar pembuangan amonia, melalui siklus urea, dimainkan oleh transaminase mitokondria.

Karbon dioksida, dalam bentuk ion bikarbonat (HCO3-), diaktifkan oleh kofaktor biotin membentuk karboksi biotin yang bereaksi dengan amonia untuk menghasilkan asam karbamat; reaksi selanjutnya menggunakan ATP untuk mentransfer fosfat ke asam karbamat membentuk karbamil fosfat dan ADP (konversi ATP menjadi ADP adalah kekuatan pendorong untuk memperoleh karboksibiotin).Fase ini dikatalisis oleh karbamil fosfat sintetase dan terjadi di mitokondria. Karbamil fosfat dan ornitin adalah substrat untuk enzim ornitin trans karbamilase yang mengubahnya menjadi citrulline; reaksi ini terjadi di mitokondria (hepatosit). Sitrulin yang dihasilkan meninggalkan mitokondria dan, di sitoplasma, berjalan di bawah "aksi"arginin suksinat sintetase: ada fusi antara kerangka karbon citrulline dan aspartat melalui serangan nukleofilik dan eliminasi air selanjutnya. Enzim arginin suksinat sintetase membutuhkan molekul ATP sehingga terjadi penggabungan energik: hidrolisis ATP menjadi AMP dan pirofosfat (yang terakhir kemudian diubah menjadi dua molekul ortofosfat) terjadi dengan pengusiran molekul d "air dari substrat dan bukan oleh aksi air medium.
"Enzim berikutnya adalah"arginin suksinase: enzim ini mampu memecah arginin suksinat menjadi arginin dan fumarat di dalam sitoplasma.
Siklus urea diselesaikan oleh enzim arginase: urea dan ornitin diperoleh; urea dibuang oleh ginjal (urin) sementara ornitin kembali ke mitokondria dan melanjutkan siklus.
Siklus urea tunduk pada modulasi tidak langsung oleh arginin: akumulasi arginin menunjukkan bahwa siklus urea harus dipercepat; modulasi arginin tidak langsung karena arginin secara positif memodulasi enzim asetil glutamat sintetase. Yang terakhir ini mampu mentransfer gugus asetil pada nitrogen glutamat: N-asetil glutamat terbentuk yang merupakan modulator langsung dari enzim karbamil-fosfo sintetase.
Arginin terakumulasi sebagai metabolit dari siklus urea jika produksi karbamil fosfat tidak cukup untuk membuang ornitin.
Urea hanya diproduksi di hati tetapi ada tempat lain di mana reaksi awal berlangsung.
Otak dan otot menggunakan strategi khusus untuk menghilangkan gugus amino. Otak menggunakan metode yang sangat efisien di mana enzim digunakan glutamin sintetase dan enzim glutamat: yang pertama hadir di neuron, sedangkan yang kedua ditemukan di hati. Mekanisme ini sangat efisien karena dua alasan:
Dua gugus amino diangkut dari otak ke hati dalam satu kendaraan;
Glutamin jauh lebih tidak beracun daripada glutamat (glutamat juga melakukan transfer saraf dan tidak boleh melebihi konsentrasi fisiologis).
Pada ikan, mekanisme serupa membawa gugus amino asam amino ke insang.
Dari otot (rangka dan jantung), gugus amino mencapai hati melalui siklus glukosa-alanin; enzim yang terlibat adalah glutamin-piruvat transaminase: memungkinkan transposisi gugus amino (yang dalam bentuk glutamat), mengubah piruvat menjadi alanin dan, pada saat yang sama, glutamat menjadi -ketoglutarat di otot dan, mengkatalisis proses sebaliknya di hati.
Transaminase dengan tugas atau posisi yang berbeda juga memiliki perbedaan struktural dan dapat ditentukan dengan elektroforesis (memiliki titik isoelektrik yang berbeda).
Adanya transaminase dalam darah dapat menjadi gejala kerusakan hati atau jantung (yaitu kerusakan jaringan pada sel hati atau jantung); transaminase berada dalam konsentrasi yang sangat tinggi baik di hati maupun di jantung: melalui elektroforesis dimungkinkan untuk menentukan apakah kerusakan telah terjadi di hati atau sel jantung.