Lihat juga: pH urin; pH vagina.
PH darah, dan cairan lainnya, mencerminkan konsentrasi ion hidrogen (H +) yang terlarut di dalamnya. Nilai pH 7 adalah netral; nilai yang lebih rendah dan lebih tinggi masing-masing bersifat asam dan basa.

Dengan meningkatkan ventilasi, yaitu frekuensi pernapasan dan/atau kedalaman napas, tubuh meningkatkan jumlah karbon dioksida yang dikeluarkan, meningkatkan pH darah, sebaliknya sebaliknya (hipoventilasi terjadi akibat alkalosis darah) .
Di ginjal ada mekanisme kompensasi lain yang sangat penting dari pH darah, bahkan jika itu jauh lebih lambat untuk bergerak. Sel-sel nefron sebenarnya dapat merespons asidosis dengan mereabsorbsi bikarbonat dalam jumlah yang lebih besar, mensekresi ion hidrogen dalam jumlah yang lebih besar, mereabsorbsi lebih banyak buffer (HCO3-) dan mendorong pembentukan amonia (yang memiliki kemampuan untuk bereaksi dengan ion H+ bebas). , membentuk ion amonium: NH3 + H + <→ NH4 +).
- HOMEOSTASIS PH DARAH TERGANTUNG PADA SISTEM BUFFER, PARU-PARU DAN GINJAL
Asidosis dan alkalosis dapat memiliki "asal respiratorik atau metabolik. Dalam kasus pertama mereka disebabkan oleh kelebihan atau cacat karbon dioksida, sedangkan pada kasus kedua mereka terkait dengan defisit atau surplus zat metabolik non-volatil, oleh karena itu tidak dapat dihilangkan. dengan nafas.
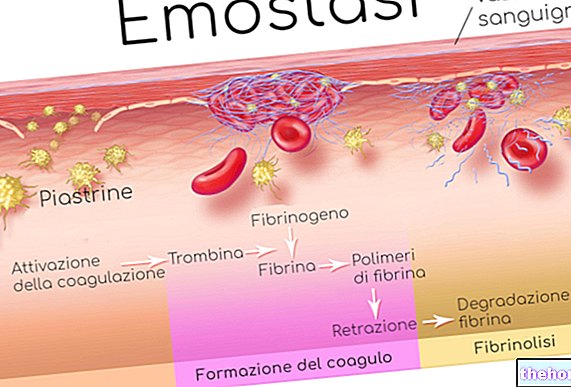
Harap dicatat: karbon dioksida itu sendiri tidak asam, karena tidak mengandung atom hidrogen. Namun, dalam lingkungan darah, karbon dioksida bergabung dengan air untuk membentuk asam karbonat, yang berdisosiasi menjadi H + dan HCO3-; menurut hukum aksi massa, jika konsentrasi karbon dioksida meningkat (lihat gambar merah), lingkungan darah menjadi diasamkan. Pada kondisi sebaliknya (warna hijau), keadaan menjadi terbalik.



- Asidosis laktat (karena hipoksia atau hipoperfusi, sering terjadi pada latihan fisik);
- Ketoasidosis (produksi besar-besaran badan keton khas diabetes), ketosis (produksi penting badan keton khas puasa berkepanjangan atau malnutrisi berat);
- Gagal ginjal;
- Peracunan;
- Diare parah;
- Hipoventilasi (disebabkan oleh obat-obatan, obat-obatan, terutama penyakit serius, PPOK dan dalam bentuk ringan juga khas pada subjek yang sangat gemuk).
- Dia muntah;
- Konsumsi berlebihan zat alkali atau obat-obatan (seperti soda kue)
- Hiperventilasi (termasuk yang diinduksi oleh obat-obatan atau pernapasan buatan atau obat-obatan).