Analisis unsur protein memberikan nilai rata-rata berikut: 55% karbon, 7% hidrogen dan 16% nitrogen; jelas bahwa protein berbeda satu sama lain, tetapi komposisi unsur rata-ratanya sedikit berbeda dari nilai yang ditunjukkan di atas .
Secara konstitusional, protein adalah makromolekul yang terbentuk dari asam -amino alami; asam amino bergabung melalui ikatan amida yang dibentuk oleh reaksi antara gugus amino dari asam a-amino dan karboksil dari asam a-amino lainnya.
Ikatan ini (-CO-NH-) juga disebut ikatan peptida karena mengikat peptida (kombinasi asam amino):
yang diperoleh adalah dipeptida karena terdiri dari dua asam amino. Karena dipeptida mengandung gugus amino bebas di satu ujung (NH2) dan karboksil di ujung lainnya (COOH), ia dapat bereaksi dengan satu atau lebih asam amino dan memperpanjang rantai baik dari kanan maupun dari kiri, dengan reaksi yang sama. terlihat di atas.
Urutan reaksi (yang, omong-omong, tidak sesederhana itu) dapat berlanjut tanpa batas: sampai ada polimer yang disebut polipeptida atau protein. Perbedaan antara peptida dan protein terkait dengan berat molekul: biasanya untuk berat molekul lebih dari 10.000 kita berbicara tentang protein.
Mengikat asam amino bersama-sama untuk mendapatkan protein kecil sekalipun adalah tugas yang sulit, meskipun baru-baru ini metode otomatis untuk memproduksi protein dari asam amino telah dikembangkan yang memberikan hasil yang sangat baik.
Oleh karena itu, protein paling sederhana terdiri dari 2 asam amino: menurut konvensi internasional, urutan penomoran asam amino dalam struktur protein dimulai dari asam amino dengan gugus a-amino bebas.
pengkodean untuk protein ini) yang menghadapi kesulitan kimia yang tidak dapat diabaikan.
Itu mungkin untuk menentukan urutan asam amino melalui degradasi Edman: protein direaksikan dengan phenylisothiocyanate (FITC), awalnya doublet nitrogen -amino menyerang phenylisothiocyanate membentuk turunan thiocarbamyl; selanjutnya, produk yang diperoleh bersiklisasi memberikan turunan feniltiohidantoin yang berfluoresen.
Edman telah merancang sebuah mesin yang disebut sequencer yang secara otomatis menyesuaikan parameter (waktu, reagen, pH, dll) untuk degradasi dan menyediakan struktur utama protein (untuk ini ia menerima Hadiah Nobel).
Struktur primer tidak cukup untuk sepenuhnya menginterpretasikan sifat-sifat molekul protein; diyakini bahwa sifat-sifat ini bergantung, dalam cara yang esensial, pada konfigurasi spasial yang cenderung diasumsikan oleh molekul protein, melipat dalam berbagai cara: yaitu, dengan asumsi apa yang telah didefinisikan sebagai struktur sekunder protein.
Struktur sekunder protein berkedip-kedip, yaitu cenderung hancur oleh pemanasan; kemudian protein terdenaturasi sendiri, kehilangan banyak sifat khasnya. Selain pemanasan di atas 70 ° C, denaturasi juga dapat disebabkan oleh penyinaran atau oleh aksi reaktan (dari asam kuat misalnya).
Denaturasi protein karena efek termal diamati, misalnya, dengan memanaskan putih telur: terlihat kehilangan penampilan agar-agarnya dan berubah menjadi zat putih yang tidak larut. Namun, denaturasi protein menyebabkan penghancuran struktur sekundernya, tetapi membiarkan struktur primernya tidak berubah (gabungan berbagai asam amino).
Protein mengambil struktur tersier ketika rantainya, meskipun masih fleksibel meskipun struktur sekundernya bengkok, terlipat sedemikian rupa sehingga menghasilkan susunan tiga dimensi yang berkerut dalam bentuk benda padat. Struktur tersier bertanggung jawab atas semua ikatan disulfida yang dapat dibentuk antara sistein -SH yang tersebar di sepanjang molekul.
Struktur kuaterner, di sisi lain, hanya milik protein yang dibentuk oleh dua atau lebih subunit. Hemoglobin, misalnya, terdiri dari dua pasang protein (yaitu, di keempat rantai protein) yang terletak di simpul tetrahedron sehingga menimbulkan struktur bola; keempat rantai protein disatukan oleh gaya ionik dan ikatan non-kovalen.
Contoh lain dari struktur kuartener adalah insulin, yang tampaknya terdiri dari sebanyak enam subunit protein yang disusun berpasangan di simpul segitiga di tengahnya adalah dua atom seng.
Protein berserat
Mereka adalah protein dengan kekakuan tertentu dan memiliki sumbu yang jauh lebih panjang dari yang lain; protein berserat yang ada dalam jumlah yang lebih besar di alam adalah kolagen (atau kolagen).
Protein berserat dapat mengasumsikan struktur sekunder yang berbeda: -helix, -sheet dan, dalam kasus kolagen, triple helix; -helix adalah struktur yang paling stabil, diikuti oleh -sheet, sedangkan yang paling tidak stabil dari ketiganya adalah triple helix.
Baik jika, mengikuti kerangka utama (berorientasi dari bawah ke atas), gerakan yang mirip dengan sekrup sekrup kanan dilakukan; sedangkan heliksnya dari tangan kiri jika gerakannya dianalogikan dengan memutar sekrup tangan kiri. Di heliks kanan, substituen -R dari asam amino tegak lurus terhadap sumbu utama protein dan menghadap ke luar, sedangkan di kiri- tangan a-heliks substituen -R menghadap ke dalam. Heliks a tangan kanan lebih stabil daripada heliks kidal karena antara vati -R c "ada interaksi yang lebih sedikit dan hambatan sterik yang lebih sedikit. Semua heliks a yang ditemukan dalam protein adalah dekstrorotal.
Struktur -helix distabilkan oleh ikatan hidrogen (jembatan hidrogen) yang terbentuk antara gugus karboksil (-C = O) dari masing-masing asam amino dan gugus amino (-NH) yang ditemukan empat residu kemudian di urutan linier.
Contoh protein yang memiliki struktur -helix adalah keratin rambut.
Dengan memperpanjang struktur -helix, transisi dari -helix ke -sheet dilakukan; juga panas atau tekanan mekanik memungkinkan untuk lulus dari -helix ke struktur -sheet.
Biasanya, dalam protein, struktur lembaran- berdekatan satu sama lain karena ikatan hidrogen antar rantai dapat dibentuk di antara bagian-bagian dari protein itu sendiri.
Dalam protein berserat, sebagian besar struktur protein diatur dalam -helix atau -sheet.
Protein globular
Mereka memiliki struktur spasial yang hampir bulat (karena banyak perubahan arah rantai polipeptida); beberapa bagian dari makhluk dapat ditelusuri kembali ke struktur -helix atau -sheet dan bagian lain tidak, sebaliknya, disebabkan oleh bentuk-bentuk ini: pengaturannya tidak acak tetapi terorganisir dan berulang.
Protein yang dimaksud sampai sekarang adalah zat dengan konstitusi yang benar-benar homogen: yaitu, urutan murni asam amino gabungan; protein seperti itu dikatakan sederhana; ada protein yang terdiri dari bagian protein dan bagian non-protein (gugus prostat) yang disebut protein mengkonjugasikan.
, di kuku, di kornea dan di lensa mata, di antara ruang interstisial beberapa organ (misalnya hati) dan seterusnya.
Strukturnya memberinya kemampuan mekanis tertentu; ia memiliki kekuatan mekanik yang besar terkait dengan elastisitas tinggi (misalnya pada tendon) atau kekakuan tinggi (misalnya pada tulang) tergantung pada fungsi yang harus dilakukan.
Salah satu sifat yang paling menarik dari kolagen adalah kesederhanaan konstitutifnya: ia terdiri dari sekitar 30% prolin dan sekitar 30% glisin; 18 asam amino lainnya hanya memiliki 40% sisa struktur protein. Urutan asam amino kolagen sangat teratur: untuk setiap tiga residu, yang ketiga adalah glisin.
Prolin adalah asam amino siklik di mana gugus R mengikat nitrogen -amino dan ini memberikan kekakuan tertentu.
Struktur terakhir adalah rantai berulang yang berbentuk "heliks; di dalam rantai kolagen, ikatan hidrogen tidak ada. Kolagen adalah "heliks tangan kiri dengan nada (panjang sesuai dengan satu putaran heliks) lebih besar dari" heliks ; heliks kolagen sangat longgar sehingga tiga rantai protein dapat saling melilit membentuk " tali tunggal: struktur triple helix.
Namun, triple helix kolagen kurang stabil dibandingkan struktur -helix dan -sheet.
Sekarang mari kita lihat mekanisme bagaimana kolagen diproduksi; pertimbangkan, misalnya, pecahnya pembuluh darah: pecahnya ini disertai dengan segudang sinyal dengan tujuan menutup pembuluh darah, sehingga membentuk gumpalan.
Koagulasi membutuhkan setidaknya tiga puluh enzim khusus. Setelah bekuan, perlu untuk melanjutkan perbaikan jaringan; Sel-sel yang dekat dengan luka juga memproduksi kolagen. Untuk melakukan ini, pertama ekspresi gen diinduksi, yaitu organisme yang dimulai dari informasi gen mampu menghasilkan protein (informasi genetik ditranskripsi pada mRNA yang meninggalkan nukleus dan mencapai ribosom di sitoplasma di mana informasi genetik diterjemahkan menjadi protein).Kemudian kolagen disintesis di ribosom (terlihat seperti heliks kiri terdiri dari sekitar 1200 asam amino dan memiliki berat molekul sekitar 150.000 d) dan kemudian terakumulasi dalam lumen di mana itu menjadi substrat bagi enzim yang mampu melakukan modifikasi pasca-translasi (modifikasi bahasa yang diterjemahkan oleh "mRNA); dalam kolagen, modifikasi ini terdiri dari hidroksilasi beberapa rantai samping, terutama prolin dan lisin.
Kegagalan enzim yang menyebabkan perubahan ini menyebabkan penyakit kudis: itu adalah penyakit yang awalnya menyebabkan pecahnya pembuluh darah, kerusakan gigi yang dapat diikuti oleh perdarahan interintestinal dan kematian; hal ini dapat disebabkan oleh penggunaan makanan yang berumur panjang secara terus menerus.
Selanjutnya, karena aksi enzim lain, modifikasi lain terjadi yang terdiri dari glikosidasi gugus hidroksil dari prolin dan lisin (gula mengikat oksigen dari OH); enzim-enzim ini ditemukan di area selain lumen oleh karena itu, protein, ketika mengalami modifikasi, bermigrasi di dalam retikulum endoplasma untuk berakhir di kantung (vesikel) yang menutup sendiri dan terlepas dari retikulum: di dalamnya terkandung pro glikosida. monomer kolagen; yang terakhir mencapai aparatus Golgi di mana enzim tertentu mengenali sistein yang ada di bagian terminal karboksi dari pro-kolagen glikosida dan menyebabkan rantai yang berbeda saling mendekat dan membentuk jembatan disulfida: dengan cara ini tiga rantai pro-kolagen terglikosidasi diperoleh dihubungkan bersama dan ini adalah titik awal di mana tiga rantai, saling berpenetrasi, kemudian, secara spontan, membentuk heliks rangkap. tersedak sendiri, melepaskan diri dari aparatus Golgi, mengangkut tiga rantai menuju pinggiran sel di mana, melalui fus ion dengan membran plasma, trimeter dikeluarkan dari sel.
Di ruang ekstra seluler, ada enzim tertentu, pro-kolagen peptidase, yang mengeluarkan dari spesies yang dikeluarkan dari sel, tiga fragmen (satu untuk setiap heliks) dari 300 asam amino l "satu, dari bagian karboksi terminal dan tiga fragmen (satu untuk setiap heliks) masing-masing sekitar 100 asam amino, dari bagian terminal amino: masih ada heliks rangkap tiga yang terdiri dari sekitar 800 asam amino per heliks yang dikenal sebagai tropokolagen.
Tropocollagen memiliki penampilan batang yang cukup kaku; trimer yang berbeda berasosiasi dengan ikatan kovalen untuk memberikan struktur yang lebih besar: mikrofibril. Dalam mikrofibril, berbagai trimer disusun secara terhuyung-huyung; banyak mikrofibril membentuk bundel tropokolagen.
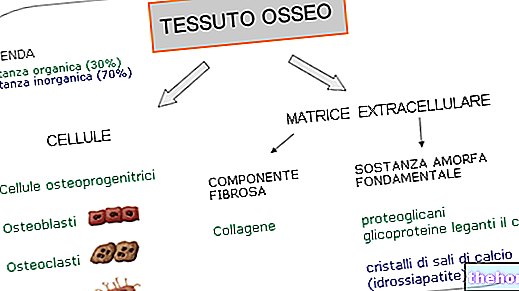
Di tulang, di antara serat kolagen, ada ruang interstisial di mana sulfat dan fosfat kalsium dan magnesium disimpan: garam ini juga menutupi semua serat; ini membuat tulang menjadi kaku.
Dalam tendon, ruang interstisial kurang kaya akan kristal daripada di tulang sementara protein yang lebih kecil hadir daripada di tropocollagen: ini memberikan elastisitas tendon.
Osteoporosis adalah penyakit yang disebabkan oleh kekurangan kalsium dan magnesium yang membuat tidak mungkin untuk memperbaiki garam di daerah interstisial dari serat tropocollagen.