Bahan aktif: Klaritromisin
Veclam 125 mg / 5 ml butiran untuk suspensi oral
Sisipan paket Veclam tersedia untuk ukuran paket:- Veclam 125 mg / 5 ml butiran untuk suspensi oral
- Veclam 250 mg / 5 ml butiran untuk suspensi oral
- Veclam tablet salut 250 mg
- Veclam tablet salut 500 mg
- Veclam RM 500 mg tablet rilis modifikasi
- Veclam 500 mg butiran untuk suspensi oral
- Veclam 500 mg / 10 ml bubuk dan pelarut untuk larutan infus
Mengapa Veclam digunakan? Untuk apa?
KATEGORI FARMAKOTERAPEUTIK
Antibakteri umum untuk penggunaan sistemik - Makrolida
INDIKASI TERAPI
Pengobatan infeksi yang disebabkan oleh patogen yang sensitif terhadap klaritromisin. Infeksi saluran rino-faring (radang amandel, faringitis), pada sinus paranasal. Otitis Media Akut (OMA). Infeksi saluran pernapasan bawah: bronkitis, pneumonia bakterial, dan pneumonia atipikal. Infeksi kulit: impetigo, erisipelas, folikulitis, furunkulosis, dan luka yang terinfeksi.
Veclam 125 mg / 5 ml butiran untuk suspensi oral diindikasikan pada anak-anak dari usia 6 bulan hingga 12 tahun.
Kontraindikasi Ketika Veclam tidak boleh digunakan
Hipersensitivitas terhadap antibiotik kelas makrolida atau salah satu eksipien yang tercantum di bagian "Komposisi".
Pemberian klaritromisin secara bersamaan dengan salah satu obat berikut dikontraindikasikan: astemizole, cisapride, pimozide, terfenadine karena dapat menginduksi perpanjangan interval QT dan aritmia jantung, termasuk takikardia ventrikel, fibrilasi ventrikel, dan torsades de pointes.
Pemberian klaritromisin bersamaan dengan ticagrelor atau ranolazine dikontraindikasikan.
Pemberian klaritromisin dan alkaloid ergot secara bersamaan (ergotamine atau dihydroergotamine) yang dapat menyebabkan toksisitas ergot dikontraindikasikan (lihat bagian "Interaksi").
Pemberian klaritromisin dan midazolam secara bersamaan untuk penggunaan oral dikontraindikasikan (lihat bagian "Interaksi").
Veclam tidak boleh digunakan pada pasien dengan perpanjangan interval QT bawaan atau didapat yang didokumentasikan dan dengan riwayat aritmia ventrikel (lihat bagian "Peringatan khusus").
Veclam tidak boleh diberikan bersamaan dengan HMG-CoA reduktase inhibitor (statin), yang dimetabolisme secara ekstensif oleh CYP3A4 (lovastatin dan simvastatin), karena peningkatan risiko miopati, termasuk rhabdomyolysis (lihat bagian "Interaksi").
Veclam tidak boleh diberikan pada pasien dengan hipokalemia (risiko pemanjangan interval QT).
Veclam tidak boleh digunakan pada pasien yang menderita insufisiensi hati parah yang terkait dengan kerusakan ginjal.
Seperti inhibitor kuat enzim CYP3A4 lainnya, klaritromisin tidak boleh digunakan bersamaan dengan colchicine (lihat bagian "Peringatan khusus").
Kewaspadaan untuk menggunakan Apa yang perlu Anda ketahui sebelum mengambil Veclam
Karena klaritromisin dimetabolisme dan diekskresikan terutama di hati, perhatian khusus harus dilakukan saat memberikan obat pada pasien dengan gangguan fungsi hati, dan pada pasien dengan gangguan ginjal sedang atau berat.
Kasus fatal gagal hati telah dilaporkan dengan penggunaan klaritromisin.Beberapa pasien mungkin memiliki penyakit hati sebelumnya atau menggunakan produk obat hepatotoksik lainnya.
Pasien harus disarankan untuk menghentikan pengobatan dan menghubungi dokter mereka jika tanda dan gejala penyakit hati seperti anoreksia, sakit kuning, urin gelap, gatal atau sakit perut terjadi.
Kasus kolitis pseudomembran telah dilaporkan dengan penggunaan hampir semua antibakteri, termasuk makrolida, mulai dari tingkat keparahan sedang hingga mengancam jiwa.Kasus diare Clostridium difficile (CDAD) telah dilaporkan.dengan penggunaan sebagian besar antibakteri, termasuk klaritromisin, yang dapat berkisar dari diare sedang hingga kolitis fatal. Pengobatan antibakteri mengubah flora usus normal, yang dapat menyebabkan proliferasi berlebihan C. difficile.
Pada semua pasien yang mengeluh diare setelah minum antibiotik, keberadaan CDAD harus dievaluasi. Pasien-pasien ini harus menjalani riwayat medis yang cermat karena telah dilaporkan bahwa CDAD dapat terjadi selama dua bulan setelah asupan antibakteri. Oleh karena itu, penghentian pengobatan klaritromisin harus dilakukan terlepas dari indikasi terapeutik. Uji mikroba harus dilakukan dan pengobatan yang tepat dimulai. Pemberian agen antiperistaltik harus dihindari.
Interaksi Obat atau makanan apa yang dapat mengubah efek Veclam
Beri tahu dokter atau apoteker Anda jika Anda baru saja mengonsumsi obat lain, bahkan obat tanpa resep dokter.
Penggunaan obat-obatan berikut ini benar-benar dikontraindikasikan karena potensi efek serius akibat interaksi obatnya: astemizole, cisapride, pimozide, terfenadine.
Asupan bersamaan mengakibatkan interval QT yang berkepanjangan, aritmia jantung termasuk takikardia ventrikel, fibrilasi ventrikel dan torsades de pointes (lihat "Kontraindikasi").
Beberapa laporan pasca pemasaran menunjukkan bahwa pemberian bersama klaritromisin dan ergotamine atau dihydroergotamine telah dikaitkan dengan toksisitas ergot akut (ergotisme) yang ditandai dengan vasospasme dan iskemia ekstremitas dan jaringan lain, termasuk sistem saraf pusat. Pemberian klaritromisin dan alkaloid ergot secara bersamaan dikontraindikasikan (lihat bagian "Kontraindikasi").
Penggunaan bersama klaritromisin dan lovastatin atau simvastatin dikontraindikasikan karena statin ini dimetabolisme secara ekstensif oleh CYP3A4 dan pengobatan bersamaan dengan klaritromisin meningkatkan konsentrasi plasmanya, yang meningkatkan risiko miopati, termasuk rhabdomiolisis (lihat bagian "Kontraindikasi").
Ada laporan rhabdomyolysis pada pasien yang memakai klaritromisin bersamaan dengan statin ini. Jika pengobatan dengan klaritromisin tidak dapat dihindari, terapi dengan lovastatin atau simvastatin harus dihentikan selama pengobatan.
Perawatan harus diambil ketika meresepkan klaritromisin dengan statin. Dalam situasi di mana penggunaan klaritromisin dan statin secara bersamaan tidak dapat dihindari, dianjurkan untuk meresepkan statin dengan dosis terdaftar terendah Kemungkinan penggunaan statin yang tidak tergantung pada metabolisme CYP3A (misalnya fluvastatin). Pasien harus dipantau untuk tanda dan gejala miopati.
Efek produk obat lain pada klaritromisin:
Obat-obatan yang menginduksi CYP3A (misalnya rifampisin, fenitoin, karbamazepin, fenobarbital, St. John's wort) dapat menginduksi metabolisme klaritromisin. Hal ini menyebabkan tingkat sub-terapeutik klaritromisin dengan kemanjuran terapeutik yang berkurang.Obat yang merupakan penginduksi kuat metabolisme sitokrom P450 seperti efavirenz, nevirapine, rifampisin, rifabutin dan rifapentin dapat mempercepat metabolisme klaritromisin dan akibatnya menurunkan kadar klaritromisin dalam plasma, sementara meningkatkan kadar plasma 14-OH-klaritromisin, suatu metabolit yang juga aktif dari sudut pandang mikrobiologis.
Sebuah studi farmakokinetik telah menunjukkan bahwa pemberian 200 mg ritonavir secara bersamaan setiap 8 jam dan 500 mg klaritromisin setiap 12 jam menyebabkan penghambatan yang nyata dari metabolisme klaritromisin. Penghambatan lengkap pembentukan 14-OH klaritromisin dicatat.
Paparan klaritromisin dikurangi dengan etravirine; namun, konsentrasi metabolit aktif, 14-OH-klaritromisin, meningkat. Sejak 14-OH-klaritromisin telah mengurangi aktivitas terhadap Mycobacterium Avium Complex (MAC), aktivitas keseluruhan terhadap patogen ini dapat diubah, oleh karena itu alternatif untuk klaritromisin harus dipertimbangkan untuk pengobatan MAC.
Pemberian flukonazol 200 mg setiap hari dan klaritromisin 500 mg dua kali sehari secara bersamaan pada 21 sukarelawan sehat menghasilkan peningkatan rata-rata konsentrasi klaritromisin minimum (Cmin) dan area di bawah kurva (AUC). ) masing-masing sebesar 33% dan 18%. Konsentrasi basal dari metabolit aktif, 14-OH-klaritromisin, tidak terpengaruh secara signifikan oleh pemberian flukonazol secara bersamaan.
Tidak ada penyesuaian dosis yang diperlukan untuk klaritromisin.
Efek klaritromisin pada produk obat lain:
Pemberian klaritromisin secara bersamaan, yang diketahui menghambat CYP3A, dan obat yang dimetabolisme terutama oleh CYP3A, dapat dikaitkan dengan peningkatan konsentrasi obat yang dapat mempotensiasi atau memperpanjang efek terapeutik dan efek samping obat yang diberikan secara bersamaan.
Klaritromisin harus digunakan dengan hati-hati pada pasien yang menerima terapi dengan obat lain yang dianggap sebagai substrat enzim CYP3A, terutama jika substrat CYP3A memiliki batas keamanan yang sempit (misalnya karbamazepin) dan / atau jika substrat dimetabolisme secara ekstensif oleh ini. enzim.
Penyesuaian dosis harus dipertimbangkan dan, bila memungkinkan, konsentrasi serum obat yang dimetabolisme terutama oleh CYP3A harus dipantau secara hati-hati pada pasien yang menerima terapi klaritromisin bersamaan.
Obat atau kelas obat yang diketahui atau diyakini dimetabolisme oleh isozim CYP3A yang sama adalah: alprazolam, antikoagulan oral (misalnya warfarin), astemizol, karbamazepin, cilostazol, cisapride, siklosporin, disopiramid, alkaloid ergot, lovastamolone, metilprednisolon rifabutin, sildenafil, simvastatin, sirolimus, tacrolimus, terfenadine, triazolam dan vinblastine, tetapi daftar ini tidak lengkap.
Obat lain yang berinteraksi dengan mekanisme serupa dalam sistem sitokrom P450 adalah fenitoin, teofilin, dan valproat. Kasus peningkatan kadar serum telah dilaporkan. Kasus lain torsades de pointes telah dilaporkan setelah penggunaan klaritromisin dan quinidin atau disopiramid secara bersamaan. Pantau konsentrasi serum obat ini saat menggunakan terapi klaritromisin.
Kasus hipoglikemia telah dilaporkan setelah penggunaan klaritromisin dan disopiramid secara bersamaan. Monitor kadar glukosa darah selama terapi. Dalam kasus penggunaan klaritromisin secara bersamaan dengan obat hipoglikemik tertentu seperti nateglinide dan repaglinide, penghambatan enzim CYP3A oleh klaritromisin dapat terjadi dan dapat menyebabkan hipoglikemia. Direkomendasikan pemantauan kadar glukosa secara hati-hati.
Omeprazol
Subyek dewasa yang sehat menerima klaritromisin (500 miligram setiap 8 jam) dalam kombinasi dengan omeprazole (40 miligram setiap hari).Konsentrasi plasma dasar omeprazole meningkat (Cmax, AUC0-24, dan T1 / 2 meningkat sebesar 30%, 89% dan 34). % masing-masing) karena pemberian klaritromisin secara bersamaan.
Nilai pH lambung rata-rata selama 24 jam adalah 5,2 ketika omeprazole diberikan sendiri, dan 5,7 ketika omeprazole diberikan bersamaan dengan klaritromisin.
Sildenafil, tadalafil dan vardenafil
Masing-masing penghambat fosfodiesterase ini dimetabolisme, setidaknya sebagian, oleh CYP3A dan CYP3A dapat dihambat oleh pemberian klaritromisin secara bersamaan. Pemberian klaritromisin dan sildenafil, tadalafil atau vardenafil secara bersamaan sangat mungkin menghasilkan peningkatan paparan inhibitor fosfodiesterase. Oleh karena itu, pengurangan dosis sildenafil, tadalafil dan vardenafil harus dipertimbangkan ketika obat ini diberikan bersama dengan klaritromisin.
Hasil studi klinis telah menunjukkan bahwa kadar plasma karbamazepin dan teofilin dapat mengalami peningkatan yang sederhana namun signifikan secara statistik ketika diberikan bersama dengan klaritromisin.
Tolterodina
Jalur metabolisme utama tolterodine melewati isoform 2D6 dari sitokrom P450 (CYP2D6). Namun, dalam subset populasi tanpa CYP2D6, jalur metabolisme yang diidentifikasi adalah CYP3A. Dalam subset populasi ini, penghambatan CYP3A menghasilkan konsentrasi serum tolterodine yang jauh lebih tinggi. . Di hadapan inhibitor CYP3A, pengurangan dosis tolterodine mungkin diperlukan serta pengurangan dosis klaritromisin pada populasi pasien di mana CYP2D6 dimetabolisme dengan buruk.
Interaksi obat lain:
Perhatian dianjurkan dalam pemberian bersamaan dengan klaritromisin dan obat ototoksik lainnya, khususnya aminoglikosida (lihat bagian "Peringatan").
Kolkisin adalah substrat dari CYP3A dan pengangkut penghabisan P-glikoprotein (Pgp). Klaritromisin dan makrolida lainnya diketahui menghambat CYP3A dan Pgp. Ketika klaritromisin dan kolkisin diberikan secara bersamaan, penghambatan CYP3A dan / atau Pgp oleh klaritromisin dapat menyebabkan peningkatan paparan colchicine. Pantau pasien untuk gejala klinis toksisitas colchicine (lihat bagian "Kewaspadaan penggunaan").
Pasien yang diobati dengan klaritromisin dan digoxin telah menunjukkan peningkatan konsentrasi serum yang terakhir, oleh karena itu kadar digoksin harus dipantau dari AZT pada kondisi mapan.
Karena klaritromisin tampaknya mengganggu penyerapan AZT yang diberikan secara bersamaan, interaksi ini dapat sangat dihindari dengan meningkatkan dosis klaritromisin dan AZT untuk memberikan interval minimal 4 jam.
Interaksi ini tidak muncul pada pasien anak dengan infeksi HIV ketika klaritromisin diberikan dalam bentuk granular bersamaan dengan AZT atau ddI.
Fenitoin dan valproat:
Ada laporan spontan atau dipublikasikan tentang interaksi inhibitor CYP3A, termasuk klaritromisin, dengan obat yang tidak dianggap dimetabolisme oleh CYP3A (misalnya fenitoin dan valproat). Penentuan tingkat serum direkomendasikan untuk obat ini bila diberikan bersamaan dengan klaritromisin. Kasus peningkatan kadar serum telah dilaporkan.
Interaksi obat dua arah:
Klaritromisin dan atazanavir, seperti itrakonazol dan saquinavir, adalah substrat dan penghambat CYP3A dan ada bukti interaksi obat dua arah antara obat ini.
Perhatian disarankan dalam pemberian bersama klaritromisin dan penghambat saluran kalsium yang dimetabolisme oleh CYP3A4 (misalnya verapamil, amlodipine, diltiazem) karena risiko hipotensi. Konsentrasi plasma klaritromisin serta penghambat saluran kalsium dapat meningkat karena interaksi Hipotensi, bradiaritmia dan asidosis laktat telah diamati pada pasien yang menggunakan klaritromisin dan verapamil secara bersamaan.
Peringatan Penting untuk diketahui bahwa:
Perhatian harus dilakukan pada pasien dengan insufisiensi ginjal berat (lihat bagian "Dosis, metode dan waktu pemberian"). Sejak klaritromisin terutama diekskresikan di hati, perhatian khusus harus dilakukan ketika memberikan antibiotik untuk pasien dengan gangguan fungsi hati dan pada subyek dengan gangguan ginjal sedang atau berat.Kasus fatal gagal hati telah dilaporkan.
Kadar plasma klaritromisin tampaknya tidak banyak berubah dengan hemodialisis atau dialisis peritoneal.
Penggunaan sebagian besar antibakteri, termasuk makrolida, dapat menyebabkan kolitis pseudomembran dan diare Clostridium difficile ringan hingga sangat parah. Kasus pasca-pemasaran toksisitas kolkisin telah dilaporkan dengan penggunaan bersama kolkisin dan klaritromisin, terutama pada pasien usia lanjut, beberapa kasus yang dilaporkan telah terjadi pada pasien dengan insufisiensi ginjal dan kematian telah dilaporkan pada beberapa pasien ini (lihat bagian "Interaksi").
Pemberian klaritromisin dan colchicine secara bersamaan merupakan kontraindikasi (lihat bagian "Kontraindikasi").
Perhatian dianjurkan dalam pemberian klaritromisin dan triazolobenzodiazepin bersamaan, seperti triazolam dan midazolam injeksi (lihat bagian "Interaksi"). Perhatian direkomendasikan dalam pemberian bersamaan dengan klaritromisin dan obat ototoksik lainnya, khususnya aminoglikosida. Oleh karena itu, disarankan untuk secara berkala memantau fungsi vestibular dan pendengaran selama dan setelah perawatan.
Karena risiko perpanjangan interval QT, klaritromisin harus digunakan dengan hati-hati pada pasien dengan penyakit arteri koroner, gagal jantung berat, hipomagnesemia, bradikardia (
Untuk mengantisipasi munculnya resistensi Streptococcus pneumoniae terhadap makrolida, penting untuk melakukan uji kerentanan sebelum meresepkan klaritromisin untuk pengobatan pneumonia yang didapat dari komunitas.Pada pneumonia yang didapat di rumah sakit, klaritromisin harus diberikan dalam kombinasi dengan antibiotik tambahan yang sesuai.
Infeksi kulit dan jaringan lunak sedang hingga sedang paling sering disebabkan oleh Staphylococcus aureus dan Streptococcus pyogenes, keduanya mungkin resisten terhadap makrolida. Maka perlu dilakukan uji kepekaan. Dalam kasus di mana antibiotik beta-laktam tidak dapat digunakan (misalnya alergi), lebih baik menggunakan antibiotik lain, seperti klindamisin.
Jika terjadi reaksi hipersensitivitas akut yang parah seperti anafilaksis, sindrom Stevens-Johnson, nekrolisis epidermal toksik dan sindrom DRESS, terapi klaritromisin harus segera dihentikan dan pengobatan yang tepat harus segera dilakukan.
Penggunaan bersamaan klaritromisin dan lovastatin atau simvastatin merupakan kontraindikasi (lihat bagian "Kontraindikasi"). Perhatian harus dilakukan saat meresepkan klaritromisin dengan statin lain. Rhabdomyolysis telah dilaporkan pada pasien yang menggunakan klaritromisin dan statin. Pasien harus dipantau untuk Tanda dan Gejala Miopati Dalam situasi di mana penggunaan klaritromisin dan statin secara bersamaan tidak dapat dihindari, dianjurkan untuk meresepkan statin dengan dosis terdaftar terendah.Kemungkinan penggunaan statin yang tidak bergantung pada metabolisme enzim CYP3A (misalnya fluvastatin) dapat dipertimbangkan (lihat bagian "Interaksi").
"Penggunaan bersamaan klaritromisin dan agen hipoglikemik oral (seperti sulfonilurea) dan / atau insulin dapat menyebabkan hipoglikemia berat. C" adalah risiko perdarahan parah dan peningkatan yang signifikan dalam rasio normalisasi internasional (INR) dan waktu protrombin ketika klaritromisin digunakan diberikan bersama dengan warfarin (lihat bagian "Interaksi").
Penggunaan obat yang berkepanjangan, mirip dengan apa yang terjadi dengan antibiotik lain, dapat menyebabkan superinfeksi dari bakteri atau jamur yang resisten. Jika superinfeksi berkembang, pengobatan harus dihentikan dan terapi yang tepat segera dimulai. Perhatian harus diberikan pada kemungkinan resistensi silang antara klaritromisin dan makrolida lainnya, linkomisin dan klindamisin.
Informasi penting tentang beberapa bahan
Veclam Granules untuk suspensi oral mengandung sukrosa. Pasien yang didiagnosis oleh dokter mereka dengan "intoleransi terhadap beberapa gula harus menghubunginya sebelum minum obat ini."
Saat meresepkan butiran Veclam untuk suspensi oral kepada pasien diabetes, kandungan sukrosa harus dipertimbangkan.
Obat ini tidak dikontraindikasikan untuk penderita penyakit celiac.
Butiran Veclam untuk suspensi oral juga mengandung minyak jarak, yang dapat menyebabkan sakit perut dan diare.
Kehamilan dan menyusui
Mintalah nasihat dokter atau apoteker Anda sebelum minum obat apa pun. Klaritromisin tidak boleh diresepkan untuk wanita hamil tanpa "penilaian manfaat / risiko yang cermat, terutama selama trimester pertama kehamilan (lihat bagian" Peringatan khusus ").
Klaritromisin diekskresikan dalam ASI dalam jumlah sedemikian rupa sehingga efek pada bayi baru lahir / bayi mungkin terjadi.
Efek pada kemampuan mengemudi dan menggunakan mesin
Tidak ada data tentang efek klaritromisin pada kemampuan mengemudi atau menggunakan mesin. Risiko vertigo, pusing, kebingungan dan disorientasi, yang mungkin terjadi setelah pemberian, harus dipertimbangkan sebelum pasien mengemudi atau mengoperasikan mesin.
Dosis dan cara penggunaan Cara menggunakan Veclam: Dosis
Anak usia 6 bulan sampai 12 tahun
Dosis harian klaritromisin yang dianjurkan pada anak usia 6 bulan sampai 12 tahun adalah 7,5 mg/kg untuk diberikan dua kali sehari untuk infeksi non-mikobakteri. Durasi pengobatan yang biasa adalah 5-10 hari tergantung pada patogen yang terlibat dan tingkat keparahan situasi.
Skema dosis Veclam 125 mg / 5 ml butiran untuk suspensi oral Penggunaan sendok:
Pembuatan suspensi : Untuk membuat suspensi Veclam tambahkan air pada butiran-butiran yang terdapat dalam botol hingga garis merah pada botol.
Kocok dengan baik. Tambahkan lebih banyak air untuk mengembalikannya ke garis.
Suspensi yang dibuat memiliki konsentrasi yang sama dengan 2,5% dan dapat disimpan pada suhu kamar selama 14 hari.
Kocok dengan baik sebelum digunakan.
Pada pasien dengan insufisiensi ginjal dengan nilai bersihan kreatinin kurang dari 30 ml / menit, dosis klaritromisin harus dikurangi setengahnya. Pada pasien ini, pengobatan tidak boleh dilanjutkan lebih dari 14 hari.
Overdosis Apa yang harus dilakukan jika Anda terlalu banyak mengonsumsi Veclam
Dalam kasus tertelan / asupan dosis berlebihan Veclam, segera beri tahu dokter Anda atau pergi ke rumah sakit terdekat.
Gangguan gastrointestinal dapat terjadi ketika dosis tinggi klaritromisin diambil. Reaksi merugikan yang terjadi pada kasus overdosis harus ditangani dengan segera menghilangkan obat yang tidak diserap dan dengan terapi suportif yang tepat.Seperti halnya makrolida lainnya, kadar klaritromisin serum tidak dihilangkan dengan hemodialisis atau dialisis peritoneal, oleh karena itu perlu dilakukan intervensi sebagai sesegera mungkin berusaha mengeliminasi obat yang belum diserap dengan bertindak secara simultan dengan terapi simtomatik yang sesuai.
Jika Anda memiliki pertanyaan tentang penggunaan Veclam, tanyakan kepada dokter atau apoteker Anda.
Efek Samping Apa efek samping dari Veclam
Seperti semua obat-obatan, Veclam dapat menyebabkan efek samping, meskipun tidak semua orang mendapatkannya. Efek samping yang dilaporkan untuk Veclam tercantum di bawah ini.
ke. Ringkasan profil keamanan
Reaksi merugikan yang paling sering dan umum terkait dengan terapi klaritromisin untuk pasien dewasa dan anak-anak adalah sakit perut, diare, mual, muntah, dan gangguan pengecapan. Efek samping ini biasanya dengan intensitas sedang dan konsisten dengan profil keamanan yang diketahui untuk antibiotik makrolida.
Tidak ada perbedaan yang signifikan dalam kejadian reaksi merugikan gastrointestinal ini selama uji klinis antara pasien dengan atau tanpa infeksi mikobakteri yang sudah ada sebelumnya.
B. Tabel ringkasan reaksi merugikan
Tabel berikut merangkum reaksi merugikan yang dilaporkan selama uji klinis dan pengalaman pasca-pemasaran dengan tablet pelepasan segera klaritromisin, butiran untuk suspensi oral dan tablet pelepasan yang dimodifikasi.
Reaksi merugikan yang dianggap mungkin terkait dengan klaritromisin dilaporkan berdasarkan jenis dan frekuensi organ, menurut konvensi berikut: sangat umum (≥1 / 10), umum (≥1 / 100,
* Karena reaksi ini telah dilaporkan secara sukarela dari populasi dengan ukuran yang tidak terbatas, tidak selalu mungkin untuk membuat perkiraan frekuensi yang benar atau menetapkan hubungan sebab-akibat dengan paparan obat. Paparan pasien melebihi satu miliar hari pasien pengobatan dengan klaritromisin
** Dalam beberapa kasus rhabdomyolysis yang dilaporkan, klaritromisin diberikan bersamaan dengan statin, fibrat, colchicine atau allopurinol.
1 Reaksi merugikan dilaporkan untuk formulasi bubuk dan pelarut hanya untuk larutan infus
2 Reaksi merugikan dilaporkan untuk butiran hanya untuk suspensi oral
3 Reaksi merugikan dilaporkan hanya untuk formulasi tablet pelepasan segera
4, 6, 8,9 Lihat paragraf a)
5, 7, 10 Lihat paragraf c)
C. Deskripsi reaksi merugikan yang dipilih
Dalam beberapa kasus rhabdomyolysis yang dilaporkan, klaritromisin diberikan bersamaan dengan statin, fibrat, colchicine atau allopurinol.
Kasus pasca pemasaran interaksi obat dan efek sistem saraf pusat (misalnya mengantuk dan kebingungan) telah dilaporkan dengan penggunaan klaritromisin dan triazolam secara bersamaan.Disarankan agar pasien dipantau untuk peningkatan efek farmakologis pada tingkat SSP.
D. Populasi anak-anak
Studi klinis telah dilakukan dengan memberikan suspensi pediatrik berbasis klaritromisin kepada anak-anak dari usia 6 bulan hingga 12 tahun. Akibatnya, anak-anak di bawah usia 12 tahun harus mengambil suspensi pediatrik.
Frekuensi, jenis dan tingkat keparahan reaksi merugikan diharapkan sebanding dengan yang terjadi pada orang dewasa.
Pelaporan efek samping
Jika Anda mendapatkan efek samping, bicarakan dengan dokter atau apoteker Anda, termasuk kemungkinan efek samping yang tidak tercantum dalam selebaran ini. Efek yang tidak diinginkan juga dapat dilaporkan secara langsung melalui sistem pelaporan nasional di "www.agenziafarmaco.gov.it/it/responsabili". Dengan melaporkan efek samping Anda dapat membantu memberikan informasi lebih lanjut tentang keamanan obat ini."
Kadaluwarsa dan Retensi
Kedaluwarsa: Lihat tanggal kedaluwarsa yang tertera pada kemasan.
Tanggal kedaluwarsa yang ditunjukkan mengacu pada produk dalam kemasan utuh, disimpan dengan benar.
Obat ini tidak memerlukan kondisi penyimpanan khusus.
PERINGATAN: Jangan gunakan obat setelah tanggal kedaluwarsa yang tertera pada kemasan.
Obat-obatan tidak boleh dibuang melalui air limbah atau limbah rumah tangga. Tanyakan apoteker Anda bagaimana cara membuang obat-obatan yang tidak lagi Anda gunakan. Ini akan membantu melindungi lingkungan.
Jauhkan obat ini dari pandangan dan jangkauan anak-anak
Komposisi dan bentuk farmasi
KOMPOSISI:
100 ml suspensi yang dilarutkan mengandung:
Bahan aktif: klaritromisin 2,5 g
Eksipien: Carbopol 974, povidone, hypromellose phthalate, minyak jarak, silika gel, sukrosa, xanthan gum, campuran rasa buah, kalium sorbat, asam sitrat, titanium dioksida, maltodekstrin, air.
BENTUK DAN ISI FARMASI
Butiran untuk suspensi oral - botol plastik 100 ml dengan dispenser.
Sumber Paket Leaflet: AIFA (Badan Obat Italia). Konten yang diterbitkan pada Januari 2016. Informasi yang ada mungkin tidak up-to-date.
Untuk memiliki akses ke versi terbaru, disarankan untuk mengakses situs web AIFA (Badan Obat Italia). Penafian dan informasi yang berguna.
01.0 NAMA PRODUK OBAT
VECLAM
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF
- Veclam tablet salut 250 mg :
Setiap tablet salut mengandung:
Prinsip aktif:
klaritromisin 250 mg.
Kandungan natrium: 3,4 mg per tablet
- Veclam tablet salut 500 mg :
Setiap tablet salut mengandung:
Prinsip aktif:
klaritromisin 500 mg.
Kandungan natrium: 6,1 mg per tablet
- Veclam 125 mg / 5 ml butiran untuk suspensi oral:
100 mL suspensi yang dilarutkan mengandung:
Prinsip aktif:
klaritromisin 2,50 g.
Eksipien dengan efek yang diketahui: sukrosa 550 mg / ml;
minyak jarak 3,2 mg/ml.
- Veclam 250 mg / 5 ml butiran untuk suspensi oral:
100 mL suspensi yang dilarutkan mengandung:
Prinsip aktif:
klaritromisin 5,00 g.
Eksipien dengan efek yang diketahui: sukrosa 455 mg / ml;
minyak jarak 6,4 mg/ml.
- Veclam 250 mg butiran untuk suspensi oral:
Setiap sachet berisi:
Prinsip aktif:
klaritromisin 250 mg.
Eksipien dengan efek yang diketahui: 1591 mg sukrosa per sachet;
minyak jarak 32,1 mg per sachet.
- Veclam 500 mg butiran untuk suspensi oral:
Setiap sachet berisi:
Prinsip aktif:
klaritromisin 500 mg.
Eksipien dengan efek yang diketahui: sukrosa 3182 mg per sachet;
minyak jarak 64,2 mg per sachet.
- Veclam 500 mg / 10 ml bubuk dan pelarut untuk larutan infus:
Setiap botol bubuk steril untuk larutan infus mengandung:
Prinsip aktif
klaritromisin 500 mg.
- Veclam RM 500 mg tablet rilis modifikasi:
Setiap tablet rilis modifikasi mengandung:
Prinsip aktif:
klaritromisin 500 mg.
Kandungan natrium 15,3 mg per tablet
Eksipien dengan efek yang diketahui: laktosa (115 mg per tablet).
Untuk daftar lengkap eksipien lihat bagian 6.1.
03.0 FORMULIR FARMASI
- Tablet berlapis.
- Butiran untuk suspensi oral.
- Bubuk dan pelarut untuk larutan infus.
- Tablet rilis yang dimodifikasi.
04.0 INFORMASI KLINIS
04.1 Indikasi Terapi
Panduan resmi tentang penggunaan yang tepat dari agen antibakteri harus dipertimbangkan.
Veclam diindikasikan pada orang dewasa dan anak-anak di atas usia 12 tahun.
Veclam 125 mg / 5 ml butiran untuk suspensi oral dan Veclam 250 mg / 5 ml butiran untuk suspensi oral diindikasikan pada anak-anak dari usia 6 bulan hingga 12 tahun.
Untuk semua bentuk farmasi:
Pengobatan infeksi yang disebabkan oleh patogen yang sensitif terhadap klaritromisin. Infeksi saluran rino-faring (radang amandel, faringitis), pada sinus paranasal. Infeksi saluran pernapasan bawah: bronkitis, pneumonia bakterial, dan pneumonia atipikal. Infeksi kulit: impetigo, erisipelas, folikulitis, furunkulosis, dan luka yang terinfeksi.
Selain itu, untuk Veclam 125 mg / 5 ml butiran untuk suspensi oral dan untuk Veclam 250 mg / 5 ml butiran untuk suspensi oral:
Otitis Media Akut (OMA).
Sebagai tambahan untuk Veclam 250 mg tablet salut dan untuk Veclam 250 mg granul untuk suspensi oral:
Infeksi odontostomatologis akut dan kronis yang ditopang oleh kuman yang sensitif.
Selain itu, untuk Veclam 500 mg tablet salut, untuk Veclam 250 mg butiran untuk suspensi oral dan untuk Veclam 500 mg butiran untuk suspensi oral:
Infeksi mikobakteri lokal atau difus yang disebabkan oleh Mycobacterium avium atau Mycobacterium intracellulare.
Infeksi lokal karena Mycobacterium chelonae, fortuitum atau kansasii.
Klaritromisin, dengan adanya pengurangan keasaman lambung, diindikasikan dalam pemberantasan Helicobacter pylori, menghasilkan penurunan konsekuen dalam kekambuhan tukak lambung.
04.2 Posologi dan cara pemberian
Pada anak di atas 12 tahun: seperti untuk orang dewasa.
Durasi pengobatan yang biasa adalah 5 sampai 14 hari, tidak termasuk pengobatan untuk pneumonia dan sinusitis yang didapat masyarakat yang memakan waktu 6 sampai 14 hari.
Pada anak di bawah usia 12 tahun: gunakan Veclam 125 mg / 5 ml butiran untuk suspensi oral atau Veclam 250 mg / 5 ml butiran untuk suspensi oral.
Durasi pengobatan yang biasa adalah 5 - 10 hari.
Penggunaan tablet salut Veclam, tablet pelepasan modifikasi Veclam atau bubuk dan pelarut Veclam untuk larutan infus tidak dianjurkan pada anak di bawah usia 12 tahun.
Veclam tablet salut 250 mg, Veclam tablet salut 500 mg, Veclam 250 mg butiran untuk suspensi oral e Veclam 500 mg butiran untuk suspensi oral:
Dosis klaritromisin yang dianjurkan pada orang dewasa dan anak di atas 12 tahun adalah 1 tablet atau 1 sachet 250 mg setiap 12 jam.
Dalam kasus infeksi berat dosis dapat ditingkatkan hingga 500 mg setiap 12 jam.
Durasi pengobatan yang biasa adalah 5 sampai 14 hari, tidak termasuk pengobatan untuk pneumonia dan sinusitis yang didapat masyarakat yang memakan waktu 6 sampai 14 hari.
Pasien dengan gangguan ginjal: pada pasien dengan insufisiensi ginjal di mana klirens kreatinin kurang dari 30 ml / menit, dosisnya harus dikurangi setengahnya, misalnya 250 mg sekali sehari atau 250 mg dua kali sehari untuk infeksi berat.
Pada pasien tersebut, pemberian tidak boleh dilanjutkan lebih dari 14 hari.
Pada pasien dengan infeksi mikobakteri, dosis awal adalah 500 mg dua kali sehari. Jika tidak ada perbaikan klinis atau bukti bakteriologis terjadi dalam waktu 3-4 minggu, dosis harian dapat ditingkatkan menjadi 1000 mg dua kali sehari.
Direkomendasikan, dalam pengobatan infeksi yang disebarkan oleh Mycobacterium Avium Complex pada pasien dengan AIDS, untuk melanjutkan pengobatan sampai hasil klinis atau mikrobiologis diperoleh dan dalam hal apapun atas kebijaksanaan dokter yang merawat Klaritromisin harus digunakan dalam kombinasi dengan lainnya obat antimikobakteri.
Pada infeksi odontostomatologis, dosis yang dianjurkan adalah 250 mg setiap 12 jam selama 5 hari.
Jadwal dosis dalam pemberantasan Helicobacter pylori:
Terapi rangkap tiga:
Klaritromisin 500 mg dua kali sehari dalam kombinasi dengan omeprazole 20 mg setiap hari dan amoksisilin 1000 mg dua kali sehari selama 7 sampai 10 hari.
Klaritromisin 500 mg dua kali sehari dalam kombinasi dengan lansoprazole 30 mg dua kali sehari dan amoksisilin 1000 mg dua kali sehari selama 10 hari.
Terapi ganda:
Klaritromisin 500 mg tiga kali sehari dalam kombinasi dengan omeprazole 40 mg setiap hari selama 14 hari, diikuti dengan omeprazole 20 mg atau 40 mg setiap hari selama 14 hari tambahan.
Klaritromisin 500 mg tiga kali sehari dalam kombinasi dengan lansoprazole 60 mg setiap hari selama 14 hari. Penekanan sekresi asam lebih lanjut mungkin diperlukan untuk pengurangan ulkus.
Klaritromisin juga telah digunakan dalam rejimen terapi berikut:
- klaritromisin + tinidazole dan omeprazole atau lansoprazole
- klaritromisin + metronidazol dan omeprazole atau lansoprazole
- klaritromisin + tetrasiklin, bismut subsalisilat, dan ranitidin
- klaritromisin + amoksisilin dan lansoprazole
- klaritromisin + ranitidine bismut sitrat
Persiapan suspensi oral dalam sachet:
Untuk membuat suspensi dalam sachet, pada saat pemberian tuangkan isi sachet ke dalam segelas air, kocok hingga diperoleh suspensi yang homogen.
Penggunaan tablet salut Veclam pada anak di bawah 12 tahun belum diteliti.
Veclam RM 500 mg tablet rilis modifikasi:
Dosis yang direkomendasikan dari Veclam RM 500 mg tablet pelepasan termodifikasi pada orang dewasa dan anak-anak di atas 12 tahun adalah 1 tablet per hari untuk dikonsumsi bersama makanan.
Dalam kasus infeksi yang lebih parah, dosisnya dapat ditingkatkan menjadi 2 500 mg tablet pelepas termodifikasi per hari untuk diminum sebagai dosis tunggal.
Tablet harus ditelan utuh.
Durasi pengobatan yang biasa adalah 5 sampai 14 hari, tidak termasuk pengobatan untuk pneumonia dan sinusitis yang didapat masyarakat yang memakan waktu 6 sampai 14 hari.
Pasien dengan gangguan ginjal: pada pasien dengan insufisiensi ginjal dengan nilai bersihan kreatinin di bawah 30 ml / menit, dosis klaritromisin harus dikurangi setengahnya, mis. 250 mg sekali sehari, atau 250 mg dua kali sehari pada infeksi berat. Pada pasien ini, pengobatan tidak boleh dilanjutkan lebih dari 14 hari. Karena tablet tidak dapat dibagi dan dosis harian 500 mg tidak dapat dikurangi, tablet pelepas modifikasi tidak boleh diberikan kepada populasi pasien ini (lihat bagian 4.3).
Penggunaan tablet pelepasan modifikasi Veclam pada anak di bawah usia 12 tahun belum diteliti.
Veclam 125 mg/5 ml butiran untuk suspensi oral dan Veclam 250 mg/5 ml butiran untuk suspensi oral:
Studi klinis telah dilakukan dengan memberikan suspensi pediatrik berbasis klaritromisin kepada anak-anak dari usia 6 bulan hingga 12 tahun. Akibatnya, anak-anak di bawah usia 12 tahun harus mengambil suspensi pediatrik (butiran untuk suspensi oral).
Dosis harian yang dianjurkan pada anak-anak adalah 7,5 mg / kg untuk diberikan dua kali sehari untuk infeksi non-mikobakteri.
Durasi pengobatan yang biasa adalah 5 - 10 hari tergantung pada patogen yang terlibat dan tingkat keparahan situasi.
Suspensi dapat diambil bersamaan dengan makanan dan dengan perut kosong dan dapat ditelan dengan susu.
Jadwal dosis Veclam 125 mg / 5 ml butiran untuk suspensi oral
Menggunakan sendok teh
Jadwal dosis Veclam 125 mg / 5 ml butiran untuk suspensi oral
Penggunaan jarum suntik dosis untuk pemberian tunggal
(Aspirasi suspensi hingga tanda kg yang sesuai)
Jadwal dosis Veclam 250 mg / 5 ml butiran untuk suspensi oral
Menggunakan sendok teh
Jadwal dosis Veclam 250 mg / 5 ml butiran untuk suspensi oral
Penggunaan jarum suntik dosis untuk pemberian tunggal
(Aspirasi suspensi hingga tanda kg yang sesuai)
Persiapan suspensi oral dalam botol:
Untuk menyiapkan suspensi Veclam:
- tambahkan air pada butiran yang terdapat dalam botol hingga garis merah pada botol.
- Kocok dengan baik.
- Tambahkan lebih banyak air untuk mengembalikannya ke garis.
Suspensi yang dibuat memiliki konsentrasi 5% untuk Veclam 250 mg/5 ml granula untuk suspensi oral dan 2,5% untuk Veclam 125 mg/5 ml granula untuk suspensi oral dan dapat disimpan pada suhu kamar (15 ° C - 30 ° C ) selama 14 hari.
Kocok dengan baik sebelum digunakan.
Menggunakan jarum suntik dosis
Buka tutup pada botol. Masukkan spuit pada leher botol dengan menggunakan adaptor khusus. Aspirasi dosis yang diinginkan yang ditunjukkan pada skala dispenser dan, setelah hanya mengambil spuit, lakukan pemberian. Kemudian, biarkan adaptor terpasang, kencangkan tutupnya kembali di leher botol.
Dosis harus dipilih dengan menggunakan skala pada jarum suntik, hingga sesuai dengan berat badan anak.
Veclam 500 mg / 10 ml bubuk dan pelarut untuk larutan infus:
Dosis yang dianjurkan pada pasien dewasa di atas 18 tahun adalah 4 - 8 mg / kg / hari dalam dua administrasi harian. Persiapan larutan yang akan disuntikkan berlangsung melalui pembubaran bubuk dalam pelarut, dan pengenceran berikutnya dalam glukosa 5% atau larutan fisiologis, sampai konsentrasi akhir 1-2 mg / ml tercapai.
Namun, disarankan untuk tidak melebihi dosis maksimum 1 g dalam dua administrasi harian.
Produk yang dilarutkan harus digunakan dalam waktu 24 jam.
Jangan gunakan larutan garam sebagai pelarut. Suntikkan dengan sangat lambat.
Pemberian harus dilanjutkan, tergantung pada tingkat keparahan infeksi, hingga 6-14 hari.
Pasien dengan gangguan ginjal: pada pasien dengan insufisiensi ginjal di mana pembersihan kreatinin kurang dari 30 ml / menit, dosisnya harus dikurangi setengahnya.
Pada pasien tersebut, pemberian tidak boleh dilanjutkan lebih dari 14 hari.
Tidak ada data yang cukup tersedia untuk merekomendasikan rejimen dosis untuk penggunaan klaritromisin IV pada pasien kurang dari 12 tahun (lihat "Veclam 125 mg / 5 ml butiran untuk suspensi oral" dan "Veclam 250 mg / 5 ml butiran untuk suspensi oral ").
Pada anak-anak antara usia 12 dan 18, dosisnya sama seperti pada orang dewasa.
04.3 Kontraindikasi
Hipersensitivitas terhadap antibiotik kelas makrolida atau salah satu eksipien yang tercantum di bagian 6.1.
- Pemberian klaritromisin secara bersamaan dengan salah satu obat berikut: astemizole, cisapride, pimozide, dan terfenadine karena dapat menginduksi pemanjangan interval QT dan aritmia jantung, termasuk takikardia ventrikel, fibrilasi ventrikel, dan torsades de pointes (lihat bagian 4.5).
- Pemberian klaritromisin bersamaan dengan ticagrelor atau ranolazine.
- Pemberian klaritromisin dan alkaloid ergot secara bersamaan (ergotamine atau dihydroergotamine), karena dapat menyebabkan toksisitas ergot (lihat bagian 4.5).
- Pemberian klaritromisin dan midazolam secara bersamaan untuk penggunaan oral (lihat bagian 4.5).
Veclam tidak boleh diberikan kepada pasien dengan riwayat perpanjangan interval QT atau aritmia ventrikel jantung, termasuk torsades de pointes (lihat bagian 4.4 dan 4.5).
Veclam tidak boleh diberikan bersamaan dengan inhibitor HMG-CoA reduktase (statin), yang dimetabolisme secara ekstensif oleh CYP3A4 (lovastatin atau simvastatin), karena peningkatan risiko miopati, termasuk rhabdomyolisis (lihat bagian 4.5).
Veclam tidak boleh diberikan pada pasien dengan hipokalemia (risiko pemanjangan interval QT).
Veclam tidak boleh digunakan pada pasien yang menderita insufisiensi hati parah yang terkait dengan kerusakan ginjal.
Seperti inhibitor kuat lainnya dari enzim CYP3A4, klaritromisin tidak boleh digunakan bersamaan dengan colchicine (lihat bagian 4.4 dan 4.5).
Karena dosis harian 500 mg tidak dapat dikurangi, tablet pelepas modifikasi Veclam dikontraindikasikan pada pasien dengan bersihan kreatinin di bawah 30 ml / menit. Semua bentuk farmasi lainnya dapat digunakan untuk kelompok pasien ini.
04.4 Peringatan khusus dan tindakan pencegahan yang tepat untuk digunakan
Tablet dan Sachet
Penggunaan terapi antibiotik apa pun, seperti dengan klaritromisin, untuk mengobati infeksi dengan: H.pylori dapat menyebabkan munculnya bakteri resisten.
Semua formulasi
Klaritromisin tidak boleh diresepkan untuk wanita hamil tanpa "penilaian manfaat / risiko yang cermat, terutama selama trimester pertama kehamilan (lihat bagian 4.6).
Seperti antibiotik lainnya, penggunaan klaritromisin yang berkepanjangan dapat menyebabkan timbulnya superinfeksi dengan bakteri dan jamur yang resisten yang memerlukan penghentian pengobatan dan penerapan terapi yang sesuai.
Perhatian harus dilakukan pada pasien yang mengalami insufisiensi ginjal berat (lihat bagian 4.2).
Kasus disfungsi hati (lihat bagian 4.8) termasuk peningkatan enzim hati, kerusakan hepatoseluler dan / atau hepatitis kolestatik, dengan atau tanpa penyakit kuning, telah dilaporkan dengan penggunaan klaritromisin. Disfungsi hati ini bisa parah dan biasanya reversibel. dilaporkan kasus gagal hati yang fatal dan biasanya dikaitkan dengan penyakit dasar yang parah atau pengobatan bersamaan.
Pasien harus disarankan untuk menghentikan pengobatan dan menghubungi dokter mereka jika tanda dan gejala penyakit hati seperti anoreksia, sakit kuning, urin gelap, gatal atau sakit perut terjadi.
Kasus kolitis pseudomembran telah dilaporkan dengan penggunaan hampir semua antibakteri, termasuk makrolida, mulai dari tingkat keparahan sedang hingga mengancam jiwa.Kasus diare Clostridium difficile (CDAD) telah dilaporkan.dengan penggunaan sebagian besar antibakteri, termasuk klaritromisin, yang dapat berkisar dari diare sedang hingga kolitis fatal. Pengobatan dengan agen antibakteri mengubah flora usus normal, yang dapat menyebabkan proliferasi berlebihan dari bakteri C. sulit. Pada semua pasien yang mengeluh diare setelah minum antibiotik, keberadaan CDAD (Clostridium difficile diare) harus dievaluasi. Pasien-pasien ini harus menjalani riwayat medis yang cermat karena telah dilaporkan bahwa CDAD dapat terjadi selama dua bulan setelah asupan agen antibakteri. Oleh karena itu, penghentian pengobatan klaritromisin harus dilakukan terlepas dari indikasi terapeutik. Uji mikroba harus dilakukan dan pengobatan yang tepat dimulai. Pemberian agen antiperistaltik harus dihindari.
Karena klaritromisin dimetabolisme dan diekskresikan terutama di hati, perhatian khusus harus dilakukan ketika memberikan obat kepada pasien dengan gangguan fungsi hati, pada pasien dengan gangguan ginjal sedang atau berat dan pada orang tua (di atas 65 tahun).
Kolkisin:
Ada laporan pasca pemasaran toksisitas kolkisin dengan penggunaan kolkisin dan klaritromisin secara bersamaan, terutama pada pasien usia lanjut, beberapa di antaranya terjadi pada pasien dengan insufisiensi ginjal. Kematian telah dilaporkan pada beberapa pasien ini (lihat bagian 4.5) Pemberian bersamaan klaritromisin dan colchicine dikontraindikasikan (lihat bagian 4.3).
Perhatian direkomendasikan dalam pemberian klaritromisin dan triazolobenzodiazepin secara bersamaan, seperti triazolam dan midazolam injeksi (lihat bagian 4.5).
Perhatian direkomendasikan dalam pemberian bersamaan dengan klaritromisin dan obat ototoksik lainnya, khususnya aminoglikosida. Oleh karena itu, disarankan untuk secara berkala memantau fungsi vestibular dan pendengaran selama dan setelah perawatan.
Karena risiko perpanjangan interval QT, klaritromisin harus digunakan dengan hati-hati pada pasien dengan penyakit arteri koroner, gagal jantung berat, hipomagnesemia, bradikardia (aritmia ventrikel sebelumnya (lihat bagian 4.3).
Radang paru-paru:
Untuk mengantisipasi munculnya perlawanan dari Streptococcus pneumoniae terhadap makrolida, penting untuk melakukan uji kepekaan sebelum meresepkan klaritromisin untuk pengobatan pneumonia yang didapat dari komunitas. Pada pneumonia yang didapat di rumah sakit, klaritromisin harus diberikan dalam kombinasi dengan antibiotik tambahan yang sesuai.
Infeksi kulit dan jaringan lunak dengan intensitas ringan hingga sedang:
Infeksi ini paling sering disebabkan oleh Stafilokokus aureus Dan Streptococcus pyogenes, keduanya mungkin resisten terhadap makrolida. Maka perlu dilakukan uji kepekaan. Dalam kasus di mana antibiotik beta-laktam tidak dapat digunakan (misalnya alergi), lebih baik menggunakan antibiotik lain, seperti klindamisin. Makrolida saat ini hanya memainkan peran mendasar dalam infeksi kulit dan jaringan lunak, seperti yang disebabkan oleh Corynebacterium minutissimum, akne vulgaris, erisipelas dan dalam situasi di mana terapi berbasis penisilin tidak dapat dilakukan.
Jika terjadi reaksi hipersensitivitas akut yang parah seperti anafilaksis, sindrom Stevens-Johnson, nekrolisis epidermal toksik dan sindrom DRESS, terapi klaritromisin harus segera dihentikan dan pengobatan yang tepat harus segera dilakukan.
Veclam harus digunakan dengan hati-hati bila diberikan bersamaan dengan produk obat yang mampu menginduksi enzim CYP3A4 (lihat bagian 4.5).
Perhatian harus diberikan pada kemungkinan resistensi silang antara klaritromisin dan makrolida lainnya, linkomisin dan klindamisin.
Penghambat reduktase HMG-CoA (statin): Penggunaan bersama klaritromisin dan lovastatin atau simvastatin merupakan kontraindikasi (lihat bagian 4.3). Perhatian harus dilakukan saat meresepkan klaritromisin dengan statin lain. Rhabdomyolysis telah dilaporkan pada pasien yang menggunakan klaritromisin dan statin. Pasien harus dipantau untuk tanda dan gejala miopati.
Dalam situasi di mana penggunaan klaritromisin dan statin secara bersamaan tidak dapat dihindari, dianjurkan untuk meresepkan statin dengan dosis terdaftar terendah.
Penggunaan statin yang tidak bergantung pada metabolisme enzim CYP3A (misalnya fluvastatin) dapat dipertimbangkan (lihat bagian 4.5).
Agen hipoglikemik oral / insulin:
Penggunaan bersama klaritromisin dan agen hipoglikemik oral (seperti sulfonilurea) dan / atau insulin dapat menyebabkan hipoglikemia berat.Direkomendasikan pemantauan glukosa ketat (lihat bagian 4.5).
Antikoagulan oral:
C "adalah risiko perdarahan hebat dan peningkatan yang signifikan dalam rasio normalisasi internasional (INR) dan waktu protrombin ketika klaritromisin diberikan bersama dengan warfarin (lihat bagian 4.5)." INR dan waktu protrombin harus sering dipantau pada pasien tersebut yang diobati secara bersamaan dengan klaritromisin dan agen antikoagulan oral.
Eksipien dengan efek yang diketahui:
Butiran veclam untuk suspensi oral mengandung sukrosa. Pasien dengan masalah herediter yang jarang dari intoleransi fruktosa, malabsorpsi glukosa-galaktosa atau insufisiensi sukrase-isomaltase tidak boleh minum obat ini.
Saat meresepkan butiran Veclam untuk suspensi oral kepada pasien diabetes, kandungan sukrosa harus dipertimbangkan.
Butiran veclam untuk suspensi oral juga mengandung minyak jarak, yang dapat menyebabkan sakit perut dan diare.
Veclam RM 500 mg tablet pelepasan termodifikasi mengandung laktosa. Pasien dengan masalah herediter yang jarang dari intoleransi galaktosa, defisiensi Lapp laktase, malabsorpsi glukosa-galaktosa tidak boleh minum obat ini.
04.5 Interaksi dengan produk obat lain dan bentuk interaksi lainnya
Penggunaan obat-obatan berikut ini benar-benar dikontraindikasikan karena potensi efek serius akibat interaksi obatnya.
Cisapride, pimozide, astemizol dan terfenadine
Peningkatan kadar cisapride terlihat pada pasien yang menggunakan cisapride dan klaritromisin secara bersamaan. Asupan bersamaan mengakibatkan interval QT yang berkepanjangan, aritmia jantung termasuk takikardia ventrikel, fibrilasi ventrikel dan torsades de pointes.Efek serupa telah diamati pada pasien yang memakai klaritromisin dan pimozide secara bersamaan (lihat bagian 4.3).
Dalam literatur dilaporkan bahwa makrolida mengubah metabolisme terfenadine dengan meningkatkan kadarnya yang kadang-kadang dikaitkan dengan aritmia jantung, seperti pemanjangan QT, takikardia ventrikel, fibrilasi ventrikel, dan torsades de pointes (lihat bagian 4.3). Dalam sebuah penelitian pada 14 sukarelawan sehat, pemberian klaritromisin dan terfenadine secara bersamaan menghasilkan peningkatan dua hingga tiga kali lipat dalam kadar serum metabolit asam terfenadine dan perpanjangan interval QT yang tidak menyebabkan efek klinis yang dapat dideteksi. Efek serupa telah dikaitkan dengan pemberian astemizol dan makrolida lainnya secara bersamaan.
Alkaloid dari ergot
Beberapa laporan pasca pemasaran menunjukkan bahwa pemberian bersama klaritromisin dan ergotamine atau dihydroergotamine telah dikaitkan dengan toksisitas ergot akut (ergotisme) yang ditandai dengan vasospasme dan iskemia ekstremitas dan jaringan lain, termasuk sistem saraf pusat. Pemberian klaritromisin dan alkaloid ergot secara bersamaan merupakan kontraindikasi (lihat bagian 4.3).
Penghambat reduktase HMG-CoA (statin)
Penggunaan klaritromisin dan lovastatin atau simvastatin secara bersamaan dikontraindikasikan (lihat bagian 4.3) karena statin ini dimetabolisme secara ekstensif oleh CYP3A4 dan pengobatan bersamaan dengan klaritromisin meningkatkan konsentrasi plasmanya, yang meningkatkan risiko miopati, termasuk rhabdomiolisis.
Ada laporan rhabdomyolysis pada pasien yang memakai klaritromisin bersamaan dengan statin ini. Jika pengobatan dengan klaritromisin tidak dapat dihindari, terapi dengan lovastatin atau simvastatin harus dihentikan selama pengobatan.
Perawatan harus diambil ketika meresepkan klaritromisin dengan statin. Dalam situasi di mana penggunaan klaritromisin dan statin secara bersamaan tidak dapat dihindari, dianjurkan untuk meresepkan statin dengan dosis terdaftar terendah Kemungkinan penggunaan statin yang tidak tergantung pada metabolisme CYP3A (misalnya fluvastatin). Pasien harus dipantau untuk tanda dan gejala miopati.
Efek produk obat lain pada klaritromisin
Obat-obatan yang menginduksi CYP3A (misalnya rifampisin, fenitoin, karbamazepin, fenobarbital, St. John's wort) dapat menginduksi metabolisme klaritromisin. Hal ini menyebabkan tingkat sub-terapeutik klaritromisin dengan kemanjuran terapeutik berkurang.
Selain itu, mungkin perlu untuk memantau konsentrasi plasma dari penginduksi CYP3A, yang dapat meningkat karena penghambatan CYP3A oleh klaritromisin (lihat juga selebaran paket inhibitor CYP3A yang diberikan).Pemberian rifabutin dan klaritromisin secara bersamaan menghasilkan peningkatan dalam kadar serum rifabutin, penurunan kadar serum klaritromisin, terkait dengan peningkatan risiko uveitis.
Obat-obatan berikut telah diketahui atau diduga mempengaruhi konsentrasi klaritromisin yang bersirkulasi; Mungkin perlu untuk menyesuaikan dosis klaritromisin atau kemungkinan menggunakan terapi alternatif dapat dipertimbangkan.
Efavirenz, nevirapine, rifampisin, rifabutin dan rifapentine
Obat-obatan yang ditemukan sebagai penginduksi kuat metabolisme sitokrom P450 seperti efavirenz, nevirapine, rifampicin, rifabutin dan rifapentine dapat mempercepat metabolisme klaritromisin dan akibatnya menurunkan kadar plasma klaritromisin sambil meningkatkan kadar plasma 14-OH-klaritromisin, a metabolit yang juga aktif dari sudut pandang mikrobiologi Karena aktivitas mikrobiologi klaritromisin dan 14-OH-klaritromisin berbeda untuk bakteri yang berbeda, efek terapeutik yang diharapkan dapat dibatalkan selama pemberian bersamaan dengan klaritromisin dan penginduksi enzim.
Etravirine
Paparan klaritromisin dikurangi dengan etravirine; namun, konsentrasi metabolit aktif, 14-OH-klaritromisin, meningkat. Sejak 14-OH-klaritromisin mengurangi aktivitas melawan Kompleks Mycobacterium Avium (MAC), aktivitas keseluruhan terhadap patogen ini dapat diubah, oleh karena itu alternatif untuk klaritromisin harus dipertimbangkan untuk pengobatan MAC.
Flukonazol
Pemberian flukonazol 200 mg setiap hari dan klaritromisin 500 mg dua kali sehari secara bersamaan kepada 21 sukarelawan sehat menghasilkan peningkatan rata-rata konsentrasi klaritromisin minimum (Cmin) dan area di bawah kurva (AUC) masing-masing sebesar 33% dan 18%. metabolit aktif, 14-OH-klaritromisin, tidak terpengaruh secara signifikan oleh pemberian flukonazol secara bersamaan.Tidak diperlukan penyesuaian dosis untuk klaritromisin. .
Ritonavir
Sebuah studi farmakokinetik telah menunjukkan bahwa pemberian bersama ritonavir 200 mg setiap 8 jam dan klaritromisin 500 mg setiap 12 jam menyebabkan penghambatan yang nyata dari metabolisme klaritromisin. Peningkatan 31% pada klaritromisin Cmax, peningkatan 182% pada Cmin dan peningkatan 77% pada AUC diamati dengan pemberian ritonavir secara bersamaan. Penghambatan lengkap pembentukan 14-OH-klaritromisin dicatat. Karena jendela terapi klaritromisin yang besar, pengurangan dosis tidak diperlukan pada pasien dengan fungsi ginjal normal. Namun, pada pasien dengan insufisiensi ginjal dan pengobatan bersamaan dengan ritonavir, penyesuaian dosis berikut harus dipertimbangkan: jika klirens kreatinin (CLCR) antara 30 dan 60 ml / menit, dosis klaritromisin harus dikurangi 50%; pada pasien yang CLCR
Penyesuaian dosis yang sama harus dipertimbangkan untuk pasien dengan gangguan fungsi ginjal yang diberikan ritonavir sebagai penambah farmakokinetik PI lainnya, termasuk atazanavir dan saquinavir (lihat Interaksi Obat Dua Arah di bawah).
Efek klaritromisin pada produk obat lain
Interaksi berbasis CYP3A
Pemberian klaritromisin secara bersamaan, yang diketahui menghambat CYP3A, dan obat yang dimetabolisme terutama oleh CYP3A, dapat dikaitkan dengan peningkatan konsentrasi obat yang dapat mempotensiasi atau memperpanjang efek terapeutik dan efek samping obat yang diberikan secara bersamaan.
Klaritromisin harus digunakan dengan hati-hati pada pasien yang menerima terapi dengan obat lain yang dianggap sebagai substrat enzim CYP3A, terutama jika substrat CYP3A memiliki batas keamanan yang sempit (misalnya karbamazepin) dan / atau jika substrat dimetabolisme secara ekstensif oleh ini. enzim.
Penyesuaian dosis harus dipertimbangkan dan, bila memungkinkan, konsentrasi serum obat yang dimetabolisme terutama oleh CYP3A harus dipantau secara hati-hati pada pasien yang menerima terapi klaritromisin bersamaan.
Obat atau kelas obat yang diketahui atau diyakini dimetabolisme oleh isozim CYP3A yang sama adalah: alprazolam, antikoagulan oral (misalnya warfarin, lihat bagian 4.4), astemizole, carbamazepine, cilostazol, cisapride, cyclosporine, disopyramide, alkaloid ergot, midazolamnisolone, methylazolamnisolone , omeprazole, pimozide, quinidine, rifabutin, sildenafil, simvastatin, sirolimus, tacrolimus, terfenadine, triazolam dan vinblastine, tetapi daftar ini tidak lengkap. Obat lain yang berinteraksi dengan mekanisme serupa melalui isozim lain dalam sistem sitokrom P450 adalah fenitoin, teofilin, dan valproat.
Antiaritmia
Kasus pasca-pemasaran torsade de pointes telah dilaporkan setelah penggunaan bersama klaritromisin dan quinidine atau disopyramide. Selama pemberian obat ini bersamaan dengan klaritromisin, perlu untuk memantau jejak elektrokardiografi untuk mendeteksi adanya perpanjangan interval QT. Pantau serum konsentrasi quinidine dan disopyramide selama digunakan dalam terapi klaritromisin.
Ada laporan pasca-pemasaran hipoglikemia setelah pemberian klaritromisin dan disopiramid secara bersamaan. Oleh karena itu kadar glukosa darah harus dipantau selama pemberian klaritromisin dan disopiramid secara bersamaan.
Agen hipoglikemik oral / Insulin
Dalam kasus penggunaan bersamaan klaritromisin dengan obat hipoglikemik tertentu seperti nateglinide dan repaglinide, penghambatan enzim CYP3A oleh klaritromisin dapat terjadi dan dapat menyebabkan hipoglikemia. Pemantauan ketat kadar glukosa dianjurkan.
Omeprazol
Subyek dewasa yang sehat menerima klaritromisin (500 miligram setiap 8 jam) dalam kombinasi dengan omeprazole (40 miligram setiap hari).Konsentrasi plasma dasar omeprazole meningkat (Cmax, AUC0-24, dan T½ meningkat masing-masing 30%, 89% dan 34%) karena dengan pemberian klaritromisin secara bersamaan.
Nilai pH lambung rata-rata selama 24 jam adalah 5,2 ketika omeprazole diberikan sendiri, dan 5,7 ketika omeprazole diberikan bersamaan dengan klaritromisin.
Sildenafil, tadalafil dan vardenafil
Masing-masing penghambat fosfodiesterase ini dimetabolisme, setidaknya sebagian, oleh CYP3A dan CYP3A dapat dihambat oleh pemberian klaritromisin secara bersamaan. Pemberian klaritromisin dan sildenafil, tadalafil atau vardenafil secara bersamaan sangat mungkin menghasilkan peningkatan paparan inhibitor fosfodiesterase. Oleh karena itu, pengurangan dosis sildenafil, tadalafil dan vardenafil harus dipertimbangkan ketika obat ini diberikan bersama dengan klaritromisin.
Teofilin, karbamazepin
Hasil studi klinis telah menunjukkan bahwa kadar plasma karbamazepin dan teofilin dapat mengalami peningkatan yang sederhana namun signifikan secara statistik (p≤0,05) ketika diberikan bersama dengan klaritromisin. Pengurangan dosis mungkin diperlukan.
Tolterodina
Jalur metabolisme utama tolterodine melewati isoform 2D6 dari sitokrom P450 (CYP2D6). Namun, dalam subset populasi tanpa CYP2D6, jalur metabolisme yang diidentifikasi adalah CYP3A. Dalam subset populasi ini, penghambatan CYP3A menghasilkan konsentrasi serum tolterodine yang jauh lebih tinggi. . Di hadapan inhibitor CYP3A, pengurangan dosis tolterodine mungkin diperlukan serta pengurangan dosis klaritromisin pada populasi pasien di mana CYP2D6 dimetabolisme dengan buruk.
Triazolobenzodiazepin (misalnya, alprazolam, midazolam, triazolam)
Ketika midazolam diberikan bersama dengan tablet klaritromisin (500 mg dua kali sehari), AUC midazolam meningkat 2,7 kali lipat setelah pemberian midazolam intravena dan 7 kali lipat setelah pemberian midazolam intravena. harus dihindari Jika midazolam intravena diperlukan bersamaan dengan klaritromisin, pasien harus dipantau secara hati-hati untuk penyesuaian dosis Tindakan pencegahan yang sama harus dilakukan pada benzodiazepin lain yang dimetabolisme oleh CYP3A, termasuk triazolam dan alprazolam. Dalam kasus benzodiazepin yang eliminasinya tidak tergantung pada CYP3A (temazepam, nitrazepam, lorazepam), interaksi yang penting secara klinis dengan klaritromisin tidak mungkin terjadi.
Interaksi obat dan efek sistem saraf pusat (SSP) (misalnya mengantuk dan kebingungan) telah dilaporkan dalam pengalaman pasca-pemasaran dengan penggunaan klaritromisin dan triazolam secara bersamaan. Dianjurkan untuk memantau pasien untuk tetap mengendalikan potensi efek farmakologis yang dapat ditentukan pada Sistem Saraf Pusat.
Interaksi obat lainnya
Aminoglikosida
Pemberian klaritromisin secara bersamaan dengan obat ototoksik lainnya harus dilakukan dengan hati-hati, khususnya dengan aminoglikosida (lihat bagian 4.4).
Kolkisin
Kolkisin adalah substrat CYP3A dan pengangkut penghabisan, P-glikoprotein (Pgp). Klaritromisin dan makrolida lainnya diketahui menghambat CYP3A dan Pgp. Ketika klaritromisin dan kolkisin diberikan secara bersamaan, penghambatan CYP3A dan / atau Pgp oleh klaritromisin dapat menyebabkan peningkatan paparan colchicine. Pantau pasien untuk gejala klinis toksisitas colchicine (lihat bagian 4.4).
Digoksin
Digoxin dianggap sebagai substrat transporter penghabisan, P-glikoprotein (Pgp). Klaritromisin diketahui menghambat Pgp. Ketika digoksin dan klaritromisin diberikan secara bersamaan, penghambatan Pgp adalah Beberapa klaritromisin dapat menyebabkan peningkatan paparan digoksin. konsentrasi digoxin plasma juga telah dilaporkan selama pengawasan pasca-pemasaran pada pasien yang menerima terapi digoxin dan klaritromisin secara bersamaan.Beberapa pasien telah menunjukkan tanda-tanda klinis yang serupa dengan mereka yang mengalami toksisitas digoxin, termasuk timbulnya aritmia yang mengancam jiwa. Konsentrasi plasma digoksin harus dipantau secara ketat saat pasien menerima terapi digoksin dan klaritromisin secara bersamaan.
Zidovudin
Pemberian bersamaan tablet klaritromisin dan AZT pada pasien dewasa dengan infeksi HIV dapat mengakibatkan penurunan konsentrasi AZT. Karena klaritromisin tampaknya mengganggu penyerapan AZT yang diberikan secara bersamaan, interaksi ini dapat sangat dihindari dengan mengubah dosis klaritromisin dan AZT untuk memberikan interval setidaknya 4 jam.Interaksi ini tidak muncul pada pasien anak dengan HIV infeksi ketika klaritromisin diambil dalam bentuk granular bersamaan dengan zidovudine atau didanosine Interaksi ini tidak mungkin terjadi ketika klaritromisin diberikan secara intravena.
Fenitoin dan valproat:
Ada laporan spontan atau dipublikasikan tentang interaksi inhibitor CYP3A, termasuk klaritromisin, dengan obat yang tidak dianggap dimetabolisme oleh CYP3A (misalnya fenitoin dan valproat). Penentuan tingkat serum direkomendasikan untuk obat ini bila diberikan bersamaan dengan klaritromisin. Kasus peningkatan kadar serum telah dilaporkan.
Interaksi Obat Dua Arah
Atazanavir
Klaritromisin dan atazanavir keduanya merupakan substrat dan penghambat CYP3A dan ada bukti interaksi obat dua arah antara obat ini.Pemberian klaritromisin secara bersamaan (500 mg dua kali sehari) dan atazanavir (400 mg sekali sehari) menghasilkan peningkatan paparan 2 kali lipat terhadap klaritromisin dan 70% penurunan paparan 14-OH-klaritromisin dengan peningkatan 28% pada AUC atazanavir. Karena jendela terapi klaritromisin yang besar, tidak diperlukan pengurangan dosis pada pasien dengan fungsi ginjal normal. Dalam kasus pasien dengan insufisiensi ginjal sedang (di mana klirens kreatinin 30 hingga 60 ml / menit), dosis klaritromisin harus dikurangi 50%, kreatinin kurang dari 30 ml / menit, dosis klaritromisin harus dikurangi dengan 75%, menggunakan formulasi klaritromisin yang sesuai. Pemberian dosis klaritromisin lebih besar dari 1000 mg per hari bersamaan dengan pemberian protease inhibitor tidak dianjurkan.
Penghambat saluran kalsium
Perhatian disarankan dalam pemberian bersama klaritromisin dan penghambat saluran kalsium yang dimetabolisme oleh CYP3A4 (misalnya verapamil, amlodipine, diltiazem) karena risiko hipotensi. Konsentrasi plasma klaritromisin serta penghambat saluran kalsium dapat meningkat karena interaksi Hipotensi, bradiaritmia dan asidosis laktat telah diamati pada pasien yang menggunakan klaritromisin dan verapamil secara bersamaan.
Itrakonazol
Klaritromisin dan itrakonazol keduanya merupakan substrat dan penghambat CYP3A, menghasilkan interaksi obat dua arah antara obat ini. Klaritromisin dapat menyebabkan peningkatan kadar plasma itrakonazol sementara itrakonazol dapat meningkatkan kadar plasma klaritromisin.Pasien yang menggunakan klaritromisin dan itrakonazol secara bersamaan harus dipantau secara hati-hati untuk tanda dan gejala potensiasi dan perpanjangan efek farmakologis obat ini.
Saquinavir
Klaritromisin dan saquinavir keduanya merupakan substrat dan penghambat CYP3A, menghasilkan "interaksi obat dua arah antara obat ini. Pemberian klaritromisin (500 mg dua kali sehari) dan saquinavir (kapsul gelatin lunak, 1200 mg tiga kali sehari) secara bersamaan pada 12 sukarelawan sehat menghasilkan nilai AUC dan Cmax saquinavir yang 177% dan 187% lebih tinggi daripada yang terlihat dengan monoterapi saquinavir.Nilai AUC dan Cmax klaritromisin sekitar 40% lebih tinggi daripada yang terlihat saat monoterapi klaritromisin diberikan. Penyesuaian dosis tidak diperlukan bila kedua obat diberikan secara bersamaan untuk jangka waktu terbatas pada dosis/formulasi yang dipelajari. Pengamatan dari studi interaksi obat yang dilakukan dengan menggunakan formulasi kapsul gelatin lunak mungkin tidak mewakili efek yang terlihat menggunakan formulasi kapsul gelatin keras saquinavir. Pengamatan dari studi interaksi obat yang dilakukan dengan saquinavir saja mungkin tidak mewakili efek yang terlihat dengan terapi kombinasi saquinavir/ritonavir. Ketika saquinavir diberikan bersamaan dengan ritonavir, pertimbangan yang cermat harus diberikan pada potensi efek ritonavir pada klaritromisin.
04.6 Kehamilan dan menyusui
Kehamilan
Keamanan klaritromisin untuk digunakan pada wanita hamil belum dievaluasi. Berdasarkan hasil yang diperoleh dari penelitian pada tikus, tikus, kelinci dan monyet, kemungkinan efek berbahaya pada perkembangan embrio-janin tidak dapat dikesampingkan. tidak direkomendasikan tanpa penilaian risiko / manfaat yang cermat.
Waktunya memberi makan
Keamanan klaritromisin untuk digunakan selama menyusui belum dievaluasi. Klaritromisin diekskresikan dalam ASI.
04.7 Efek pada kemampuan mengemudi dan menggunakan mesin
Tidak ada data tentang efek klaritromisin pada kemampuan mengemudi atau menggunakan mesin. Risiko pusing, vertigo, kebingungan dan disorientasi, yang mungkin terjadi setelah pemberian, harus dipertimbangkan sebelum pasien mengemudi atau menggunakan mesin.
04.8 Efek yang tidak diinginkan
ke. Ringkasan profil keamanan
Reaksi merugikan yang paling sering dan umum terkait dengan terapi klaritromisin untuk pasien dewasa dan anak-anak adalah sakit perut, diare, mual, muntah, dan gangguan pengecapan. Efek samping ini biasanya dengan intensitas sedang dan konsisten dengan profil keamanan yang diketahui untuk antibiotik makrolida (lihat bagian b dari bagian 4.8).
Tidak ada perbedaan yang signifikan dalam kejadian reaksi merugikan gastrointestinal ini selama uji klinis antara pasien dengan atau tanpa infeksi mikobakteri yang sudah ada sebelumnya.
B. Tabel ringkasan reaksi merugikan
Tabel berikut merangkum reaksi merugikan yang dilaporkan selama studi klinis dan pengalaman pasca-pemasaran dengan tablet pelepasan segera klaritromisin, butiran untuk suspensi oral, bubuk dan pelarut untuk larutan infus dan tablet pelepasan yang dimodifikasi.
Reaksi merugikan yang dianggap mungkin terkait dengan klaritromisin dilaporkan berdasarkan jenis dan frekuensi organ, menurut konvensi berikut: sangat umum (≥1 / 10), umum (≥1 / 100,
* Karena reaksi ini telah dilaporkan secara sukarela dari populasi dengan ukuran yang tidak terbatas, tidak selalu mungkin untuk membuat perkiraan frekuensi yang benar atau menetapkan hubungan sebab-akibat dengan paparan obat. Paparan pasien melebihi satu miliar hari pasien pengobatan dengan klaritromisin
** Dalam beberapa kasus rhabdomyolysis yang dilaporkan, klaritromisin diberikan bersamaan dengan statin, fibrat, colchicine atau allopurinol.
1 Reaksi merugikan dilaporkan untuk formulasi bubuk dan pelarut hanya untuk larutan infus
2 Reaksi merugikan dilaporkan untuk butiran hanya untuk suspensi oral
3 Reaksi merugikan dilaporkan hanya untuk formulasi tablet pelepasan segera
4, 6, 8,9 Lihat paragraf a)
5, 7, 10 Lihat paragraf c)
C. Deskripsi reaksi merugikan yang dipilih
Flebitis tempat suntikan, nyeri tempat suntikan, nyeri tusukan jarum dan peradangan tempat suntikan khusus untuk formulasi intravena.
Dalam beberapa kasus rhabdomyolysis yang dilaporkan, klaritromisin diberikan bersamaan dengan statin, fibrat, colchicine atau allopurinol (lihat bagian 4.3 dan 4.4).
Ada laporan pasca pemasaran tentang interaksi obat dan efek Sistem Saraf Pusat (SSP) (misalnya mengantuk dan kebingungan) dengan penggunaan klaritromisin dan triazolam secara bersamaan. Disarankan agar pasien dipantau untuk peningkatan efek farmakologis pada tingkat SSP (lihat bagian 4.5).
Kasus langka tablet pelepasan modifikasi klaritromisin dalam tinja telah dilaporkan, sebagian besar terjadi pada pasien dengan perubahan anatomi (termasuk ileostomi atau kolostomi) atau gangguan fungsi gastrointestinal dengan waktu transit gastrointestinal yang lebih pendek. Dalam beberapa kasus, residu tablet telah terjadi dalam konteks diare. Untuk pasien yang telah mengalami adanya residu tablet dalam tinja dan tidak ada perbaikan dalam kondisi mereka, perubahan formulasi klaritromisin yang berbeda (misalnya suspensi oral) atau antibiotik lain dianjurkan.
Populasi khusus: Reaksi merugikan pada pasien immunocompromised (lihat bagian e).
D. Populasi anak-anak
Studi klinis telah dilakukan dengan memberikan suspensi pediatrik berbasis klaritromisin kepada anak-anak dari usia 6 bulan hingga 12 tahun. Akibatnya, anak-anak di bawah usia 12 tahun harus mengambil suspensi pediatrik. Tidak ada cukup data yang tersedia untuk merekomendasikan rejimen dosis untuk penggunaan klaritromisin IV pada pasien kurang dari 12 tahun.
Frekuensi, jenis dan tingkat keparahan reaksi merugikan diharapkan sebanding dengan yang terjadi pada orang dewasa.
Dan. Populasi khusus lainnya
Pasien immunocompromised
Pada pasien AIDS atau immunocompromised yang dirawat karena infeksi mikobakteri dengan klaritromisin dosis tinggi untuk waktu yang lama, seringkali sulit untuk membedakan reaksi merugikan yang mungkin terkait dengan pemberian klaritromisin dari human immunodeficiency virus (HIV) atau manifestasi terkait penyakit penyerta. .
Pada pasien dewasa, reaksi merugikan yang paling sering dilaporkan oleh pasien yang diobati dengan total dosis harian 1000 mg dan 2000 mg klaritromisin adalah: mual, muntah, gangguan rasa, sakit perut, diare, ruam, perut kembung, sakit kepala, sembelit, gangguan pendengaran, peningkatan serum Glutamic-Oxaloacetic Transaminase (SGOT) dan Serum Glutamic-Pyruvic Transaminase (SGPT). Reaksi tambahan yang lebih jarang termasuk dyspnoea, insomnia dan mulut kering. Insidennya sebanding untuk pasien yang diobati dengan 1000 mg dan 2000 mg, tetapi umumnya 3 sampai 4 kali lebih sering pada pasien yang menerima dosis harian total klaritromisin 4000 mg.
Pada pasien immunocompromised ini, evaluasi nilai laboratorium dilakukan dengan menganalisis nilai-nilai di luar tingkat abnormal yang dianggap serius untuk tes tertentu (misalnya batas atas dan bawah). Berdasarkan kriteria ini, sekitar 2% atau 3% pasien yang mengonsumsi 1000 mg atau 2000 mg klaritromisin setiap hari memiliki SGOT dan SGPT abnormal yang sangat tinggi, dan jumlah sel darah putih dan trombosit yang sangat rendah. Persentase pasien yang lebih rendah yang termasuk dalam dua kelompok dosis ini juga menunjukkan peningkatan nilai BUN. Insiden nilai abnormal yang sedikit lebih tinggi dicatat pada pasien yang diobati dengan 4000 mg klaritromisin setiap hari untuk semua parameter tidak termasuk formula leukosit.
Pelaporan dugaan reaksi merugikan.
Pelaporan dugaan reaksi merugikan yang terjadi setelah otorisasi produk obat penting karena memungkinkan pemantauan berkelanjutan dari keseimbangan manfaat / risiko produk obat. Profesional kesehatan diminta untuk melaporkan setiap dugaan reaksi merugikan melalui sistem pelaporan nasional. "alamat https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Overdosis
Dalam kasus klaritromisin dosis tinggi, gangguan pencernaan dapat terjadi. Seorang pasien yang menderita gangguan bipolar menelan delapan gram klaritromisin yang menunjukkan perubahan status mental, perilaku paranoid, hipokalemia, hipoksemia. Reaksi merugikan yang terjadi pada kasus overdosis harus ditangani dengan eliminasi segera obat yang tidak diserap dan terapi suportif yang tepat.Seperti makrolida lainnya, kadar klaritromisin serum tidak dihilangkan dengan hemodialisis atau dialisis peritoneal.
Dalam kasus overdosis, pengobatan dengan klaritromisin IV (bubuk dan pelarut untuk larutan infus) harus dihentikan dan semua tindakan suportif yang tepat harus dilakukan.
05.0 SIFAT FARMAKOLOGIS
05.1 Sifat farmakodinamik
Kelompok farmakoterapi: antibakteri umum untuk penggunaan sistemik - makrolida.
Kode ATC: J01FA09.
Klaritromisin adalah makrolida baru yang dikembangkan oleh Abbott, yang dihasilkan dari substitusi pada posisi 6 di cincin lakton eritromisin dari gugus hidroksil dengan gugus CH3O.
Makrolida baru telah terbukti memiliki spektrum antibakteri in vitro yang aktif melawan bakteri Gram positif dan Gram negatif yang paling terkenal dan penting secara klinis, termasuk aerob dan anaerob.
Spektrum antibakteri klaritromisin secara in vitro ditemukan sebagai berikut: Streptococcus agalactiae, Streptococcus pyogenes, Streptococcus viridans, Streptococcus pneumoniae, Haemophilus influenzae, Haemophilus parainfluenzae, Neisseria gonorrheaopleae, Listeria monocyasmae, Legacterionella pneumoniajuni, Chacterionella pneumoniae Staphilococco aureus, Propionibacterium acnes, Mycobacterium avium, Mycobacterium leprae, Mycobacterium intracellulare, Mycobacterium chelonae, Mycobacterium fortuitum dan Mycobacterium kansasii.
Tindakannya terjadi dengan mengikat subunit ribosom 50S, menghambat sintesis protein sel bakteri.
BREAKPOIN
Komite Eropa untuk Tes Sensitivitas Antimikroba (EUCAST) telah menetapkan breakpoints berikut untuk klaritromisin, memisahkan organisme yang rentan.
Klaritromisin digunakan untuk "pemberantasan"H. pylori: konsentrasi hambat minimum (MIC) 0,25 mcg / ml yang telah ditetapkan sebagai titik henti sensitivitas oleh Clinical and Laboratory Standards Institute (C.I.S.I).
05.2 Sifat farmakokinetik
Studi pada anjing telah menunjukkan bahwa setelah pemberian intravena atau oral 10 mg / kg ada konsentrasi obat plasma 3, 2 atau 1 mg / ml pada 1, 4 dan 12 jam, masing-masing.
Dalam 5 hari pemberian klaritromisin berlabel (14C) secara oral atau intravena, sekitar 35-36% dari dosis 14C ditemukan dalam urin dan sekitar 52% di feses.
Klaritromisin dimetabolisme di hati dan metabolit terpenting adalah klaritromisin 14-hidroksi-N-demetil yang mencapai konsentrasi plasma puncak 0,5 mcg/ml dan 1,2 mcg/ml setelah 2-4 jam setelah pemberian 250 dan 1200 mg. Hanya setelah asupan oral 1200 mg juga ditemukan kadar descladinosil-clarithromycin yang rendah dalam plasma; proses metabolisme cenderung jenuh pada dosis tinggi.
Studi farmakokinetik pada manusia telah menunjukkan konsentrasi plasma puncak 2,08 g / ml setelah pemberian oral 250 mg klaritromisin.
Setelah pemberian intravena klaritromisin 500 mg berarti puncak plasma 5,52 ± 0,98 mcg / ml tercapai.
Waktu paruh senyawa sama dengan 6,3 jam.
Metabolit yang sama yang terbentuk setelah pemberian oral diidentifikasi, tetapi dalam konsentrasi yang lebih rendah, mungkin sehubungan dengan tidak adanya metabolisme lintas pertama di hati.
Formulasi rilis yang dimodifikasi:
Farmakokinetik klaritromisin pelepasan termodifikasi yang diberikan secara oral dipelajari pada pasien dewasa dan dibandingkan dengan klaritromisin 250 mg dan 500 mg tablet pelepasan segera. Ketika total dosis harian yang sama diberikan, tingkat penyerapan setara. Bioavailabilitas absolut adalah sekitar 50%.
Setelah beberapa dosis, sedikit akumulasi ditemukan dan metabolisme tidak berubah pada spesies apa pun.
Berdasarkan hasil penyerapan ekivalen, data formulasi pelepasan termodifikasi berikut ini dapat diterapkan secara in vitro dan in vivo.
In vitro
Studi in vitro telah menunjukkan bahwa pengikatan protein klaritromisin dalam plasma manusia rata-rata sekitar 70%. pada konsentrasi 0,45 – 4,5 mcg/ml. Penurunan pengikatan hingga 41% pada konsentrasi 45 mcg/ml menunjukkan bahwa tempat pengikatan dapat menjadi jenuh, namun hal ini hanya terjadi pada konsentrasi obat tinggi yang jauh dari tingkat terapeutik.
in vivo
Di semua jaringan, konsentrasi klaritromisin, tidak termasuk sistem saraf pusat, jauh lebih tinggi daripada konsentrasi obat yang bersirkulasi.
Konsentrasi tertinggi ditemukan pada jaringan hati dan paru-paru, dimana rasio jaringan/plasma adalah 10 sampai 20.
Perilaku farmakokinetik klaritromisin tidak linier. Pada pasien yang makan dan menerima klaritromisin pelepasan termodifikasi 500mg / hari, konsentrasi plasma puncak klaritromisin dan 14-OH klaritromisin masing-masing adalah 1,3 mcg / ml dan 0,48 mcg / ml.Ketika dosis ditingkatkan hingga 1000 mg / hari, nilai konsentrasi kondisi tunak masing-masing adalah 2,4 mcg / mL dan 0,67 mcg / mL.
Klaritromisin dimetabolisme di hati oleh sitokrom P450. Tiga metabolit telah dijelaskan: N-demethyl-clarithromycin; decladinosil-klaritromisin dan 14-hidroksi-klaritromisin.
Waktu paruh klaritromisin dan metabolit aktifnya masing-masing adalah 5,3 dan 7,7 jam.
Pada konsentrasi yang lebih tinggi, waktu paruh klaritromisin dan metabolitnya cenderung lebih lama.
Klaritromisin diekskresikan melalui urin (sekitar 40%) dan feses (sekitar 30%).
05.3 Data keamanan praklinis
LD50 pada mencit dan mencit lebih besar dari 5 g/kg per oral dan lebih besar dari 300 mg/kg per oral pada anjing dan monyet. Toksisitas jangka pendek (1 bulan) tidak menunjukkan efek toksik, baik pada tikus (150 mg/kg/hari), maupun pada anjing (10 mg/kg/hari). Selanjutnya toksisitas kronis (3 bulan) adalah 15 mg/kg/hari pada tikus dan 10 mg/kg/hari pada anjing.
Uji mutagenisitas telah menunjukkan bahwa obat tersebut tidak memiliki efek mutagenik atau aktivasi mikrosomal. Klaritromisin tidak berpengaruh pada aktivitas motorik tikus setelah pemberian oral 100 mg / kg.
06.0 INFORMASI FARMASI
06.1 Eksipien
Veclam tablet salut 250 mg:
Natrium kroskarmelosa, pati pragelatinisasi, selulosa mikrokristalin, E-104, gel silika, povidone, asam stearat, magnesium stearat, bedak, hypromellose, propilen glikol, sorbitan monoleat, vanillin, E-171, hidroksipropil selulosa, asam sorbat.
- Veclam tablet salut 500 mg :
Natrium kroskarmelosa, selulosa mikrokristalin, gel silika, povidon, asam stearat, magnesium stearat, bedak; larutan pelapis: hypromellose, hidroksipropilselulosa, propilen glikol, sorbitan monoleat, E-171, asam sorbat, vanillin, E-104.
- Veclam 125 mg / 5 ml butiran untuk suspensi oral dan Veclam 250 mg / 5 ml butiran untuk suspensi oral:
Carbopol 974, povidone, hypromellose phthalate, minyak jarak, silika gel, sukrosa, xanthan gum, campuran rasa buah, kalium sorbat, asam sitrat, titanium dioksida, maltodekstrin, air.
- Veclam 500 mg / 10 ml bubuk dan pelarut untuk larutan infus:
Asam laktobionat, natrium hidroksida sebagai pengatur pH.
Setiap botol pelarut mengandung:
Air p.p.i.
- Veclam 250 mg butiran untuk suspensi oral dan Veclam 500 mg butiran untuk suspensi oral:
Carbopol 974P, povidone K90, hidroksipropil metilselulosa ftalat, minyak jarak, silikon dioksida, maltodekstrin, sukrosa, titanium dioksida, pati termodifikasi, rasa jeruk, amonium terglisirizinasi, asesulfam K.
- Veclam RM 500 mg tablet rilis modifikasi:
Asam sitrat anhidrat, natrium alginat, natrium dan kalsium alginat, laktosa, povidone K30, bedak, asam stearat, magnesium stearat, hypromellose 6cps, makrogol 400, makrogol 8000, titanium dioksida (E-171), asam sorbat, kuinolin kuning (E - 104).
06.2 Ketidakcocokan
Saat ini tidak ada inkompatibilitas spesifik dengan obat yang diketahui.
06.3 Masa berlaku
Veclam tablet salut 250 mg 3 tahun.
Veclam tablet salut 500 mg 3 tahun.
Veclam 125 mg / 5 ml butiran untuk suspensi oral 2 tahun.
Veclam 250 mg / 5 ml butiran untuk suspensi oral 2 tahun.
Veclam 250 mg butiran untuk suspensi oral 3 tahun.
Veclam 500 mg butiran untuk suspensi oral 3 tahun.
Veclam 500 mg / 5 ml bubuk dan pelarut untuk larutan infus 3 tahun.
Veclam RM 500 mg tablet rilis modifikasi 3 tahun.
06.4 Tindakan pencegahan khusus untuk penyimpanan
Untuk kemasan butiran 500 mg untuk suspensi oral: Simpan pada suhu tidak melebihi 25 ° C.
Untuk ukuran kemasan tablet salut 250 mg, tablet salut 500 mg, tablet lepas modifikasi RM 500, butiran 250 mg untuk suspensi oral, butiran 125 mg / 5 ml untuk suspensi oral dan butiran 250 mg / 5 ml untuk suspensi oral: Produk obat ini tidak tidak memerlukan kondisi penyimpanan khusus.
Untuk kemasan 500 mg / 10 ml bubuk dan pelarut untuk larutan infus: Tidak ada tindakan pencegahan khusus untuk penyimpanan. Produk yang dilarutkan harus digunakan dalam waktu 24 jam.
06.5 Sifat kemasan langsung dan isi kemasan
- Veclam tablet salut 250 mg :
Kotak karton berisi 12 bungkus blister
- Veclam tablet salut 500 mg :
Kotak karton berisi blister buram 14 sel
- Veclam RM 500 mg tablet rilis modifikasi:
Kotak karton berisi kemasan blister 7 sel
- Veclam 125 mg / 5 ml butiran untuk suspensi oral:
Botol plastik 100 ml dengan dispenser
- Veclam 250 mg / 5 ml butiran untuk suspensi oral:
Botol plastik 100 ml dengan dispenser
- Veclam 500 mg / 10 ml bubuk dan pelarut untuk larutan infus:
Kotak karton berisi 1 ampul klaritromisin 500 mg + 1 ampul pelarut
- Veclam 250 mg butiran untuk suspensi oral:
Kardus isi 14 sachet 250 mg
- Veclam 500 mg butiran untuk suspensi oral:
Kotak karton isi 14 sachet 500 mg
06.6 Petunjuk penggunaan dan penanganan
Lihat bagian 4.2
07.0 PEMEGANG OTORITAS PEMASARAN
MALESCI Pharmacobiological Institute S.p.A. Via Lungo l "Ema, 7 - Bagno a Ripoli (FI)
Di bawah lisensi dari ABBOTT S.r.l. - Campoverde di Aprilia (LT)
08.0 NOMOR OTORITAS PEMASARAN
Veclam tablet salut 250 mg:
Blister 12 tablet - AIC 027529054
Veclam tablet salut 500 mg:
Blister 14 tablet - AIC 027529116
Veclam 125 mg / 5 ml butiran untuk suspensi oral:
Botol 100 ml - AIC 027529041
Veclam 250 mg / 5 ml butiran untuk suspensi oral:
Botol 100 ml - AIC 027529104
Veclam 250 mg butiran untuk suspensi oral:
14 Sachet - AIC 027529080
Veclam 500 mg butiran untuk suspensi oral:
14 Sachet - AIC 027529092
Veclam 500 mg / 10 ml bubuk dan pelarut untuk larutan infus:
Botol + botol pelarut - AIC 027529039
Veclam RM 500 mg tablet rilis modifikasi:
Blister dari 7 tablet rilis yang dimodifikasi - AIC n. 027529130
09.0 TANGGAL OTORISASI PERTAMA ATAU PEMBARUAN KUASA
Veclam tablet salut 250 mg 19/02/1997
Veclam 500 mg tablet salut 06/03/1999
Veclam 125 mg / 5 ml butiran untuk suspensi oral 19/02/1997
Veclam 500 mg / 10ml bubuk dan pelarut untuk larutan infus 04/01/1992
Veclam 250 mg / 5 ml butiran untuk suspensi oral 17/08/1999
Veclam 250 mg butiran untuk suspensi oral 17/03/1999
Veclam 500 mg butiran untuk suspensi oral 17/03/1999
Veclam RM 500 mg tablet rilis modifikasi 30/05/2001
Perpanjangan otorisasi: 31/05/2010
10.0 TANGGAL REVISI TEKS
Penetapan AIFA April 2015











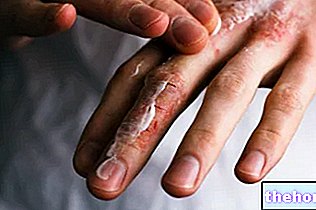



.jpg)





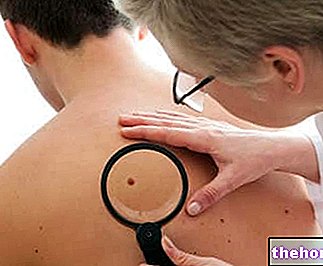
.jpg)





